题目内容
0.2L 1mol/LFeCl3与0.3L 1mol/LMgCl2两溶液中,Cl-的物质的量浓度之比为( )
| A、3:2 | B、1:1 |
| C、2:3 | D、1:3 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:根据盐溶液中氯离子的物质的量浓度=化学式中氯离子的个数×溶液的物质的量浓度计算即可.
解答:
解:FeCl3溶液中氯离子的物质的量浓度=3×c( FeCl3)=3×1mol/L=3mol/L,
MgCl2溶液中氯离子的物质的量浓度=2×c(MgCl2)=2×1mol/L=2mol/L,
所以0.2L 1mol/LFeCl3与0.3L 1mol/LMgCl2两溶液中,Cl-的物质的量浓度之比3:2.
故选A.
MgCl2溶液中氯离子的物质的量浓度=2×c(MgCl2)=2×1mol/L=2mol/L,
所以0.2L 1mol/LFeCl3与0.3L 1mol/LMgCl2两溶液中,Cl-的物质的量浓度之比3:2.
故选A.
点评:本题考查了溶液中离子的物质的量浓度的计算,难度不大,明确溶液中离子的浓度与溶液的浓度和物质的化学式有关,与溶液的体积无关.

练习册系列答案
相关题目
有关化学用语表达,下列正确的是( )
A、CS2的比例模型: |
B、铍原子最外层的电子云图: |
| C、石英的分子式:SiO2 |
D、氮原子最外层轨道表示式: |
下列说法正确的是( )
| A、SO3溶于水后能导电,故SO3为电解质 |
| B、强电解质的水溶液中不存在大量溶质分子 |
| C、向NaCN溶液中滴入酚酞试液显红色,则HCN为强酸 |
| D、25℃时,用CH3COOH溶液滴定等浓度NaOH溶液至pH=7,V(CH3COOH)<V(NaOH) |
下列有关说法错误的是( )
| A、常用丁达尔效区分溶液与胶体 |
| B、在铜锌原电池中,负极上发生Zn-2e-═Zn2+ |
| C、常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均减少 |
| D、向AgCl沉淀中滴加KI溶液,沉淀变为黄色,说明Ksp(AgCl)>Ksp(AgI) |
下列各组离子在水溶液中能够大量共存的是( )
| A、OH-、SO42-、Fe3+ |
| B、NH4+、OH-、NO3- |
| C、Na+、Cl-、SO42- |
| D、H+、HCO3-、K+ |
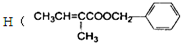 是一种的香精素,有关合成路线如下:
是一种的香精素,有关合成路线如下: