题目内容
下列有关说法错误的是( )
| A、常用丁达尔效区分溶液与胶体 |
| B、在铜锌原电池中,负极上发生Zn-2e-═Zn2+ |
| C、常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均减少 |
| D、向AgCl沉淀中滴加KI溶液,沉淀变为黄色,说明Ksp(AgCl)>Ksp(AgI) |
考点:胶体的重要性质,原电池和电解池的工作原理,弱电解质在水溶液中的电离平衡,难溶电解质的溶解平衡及沉淀转化的本质
专题:基本概念与基本理论
分析:A.区分胶体和溶液的方法为丁达尔效应;
B.锌电极作负极,失电子;
C.由NH3.H2O?OH-+NH4+可知,n(OH-)增大,但溶液的体积增大的多,则c(OH-)减小;
D.沉淀向更难溶的方向转化.
B.锌电极作负极,失电子;
C.由NH3.H2O?OH-+NH4+可知,n(OH-)增大,但溶液的体积增大的多,则c(OH-)减小;
D.沉淀向更难溶的方向转化.
解答:
解:A.胶体有丁达尔效应,溶液无丁达尔效应,故A正确;
B.在铜锌原电池中,锌电极上发生的反应为Zn-2e-=Zn2+,故B正确;
C.用水稀释0.1mol/L氨水时,溶液中随着水量的增加,由NH3.H2O?OH-+NH4+可知,n(OH-)增大,但溶液的体积增大的多,则c(OH-)减小,c(H+)增大,故C错误;
D.沉淀向更难溶的方向转化,沉淀变为黄色,说明Ksp(AgCl)>Ksp(AgI),故D正确.
故选C.
B.在铜锌原电池中,锌电极上发生的反应为Zn-2e-=Zn2+,故B正确;
C.用水稀释0.1mol/L氨水时,溶液中随着水量的增加,由NH3.H2O?OH-+NH4+可知,n(OH-)增大,但溶液的体积增大的多,则c(OH-)减小,c(H+)增大,故C错误;
D.沉淀向更难溶的方向转化,沉淀变为黄色,说明Ksp(AgCl)>Ksp(AgI),故D正确.
故选C.
点评:本题考查胶体的性质、电解原理、电解质的电离一级沉淀变化等,难度不大,学习中注意相关基础知识的积累.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
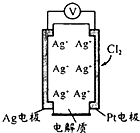 利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体
利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体物质.下列分析不正确的是( )
| A、电子经外电路流向Pt电极 |
| B、电池工作时,电解质中Ag+数目减少 |
| C、正极反应:C12+2e-+2Ag+=2AgCl |
| D、空气中c(C12)越大,Ag极消耗速率越快 |
0.2L 1mol/LFeCl3与0.3L 1mol/LMgCl2两溶液中,Cl-的物质的量浓度之比为( )
| A、3:2 | B、1:1 |
| C、2:3 | D、1:3 |
如图图象不能正确反映其对应实验操作的是( )
A、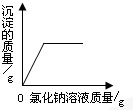 向一定量的硝酸银溶液中逐滴加入氯化钠溶液 |
B、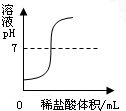 向一定量的氢氧化钠溶液中逐滴加入稀盐酸 |
C、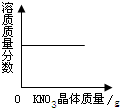 向t℃的饱和硝酸钾溶液中加入一定量的硝酸钾晶体 |
D、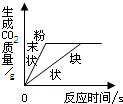 等质量的碳酸钙分别与等体积等质量分数的足量稀盐酸反应 |
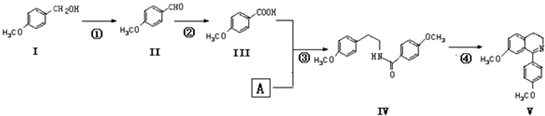
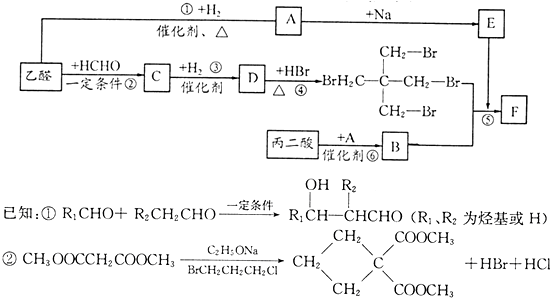
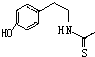 )在一定条件下也能发生类似上述第④步骤的环化反应,化合物Ⅶ环化反应产物的结构简式为
)在一定条件下也能发生类似上述第④步骤的环化反应,化合物Ⅶ环化反应产物的结构简式为