题目内容
20.下列有机物一氯代物的同分异构体数目与其他三种不同的是( )| A. | 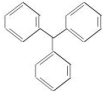 | B. | 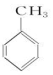 | C. | 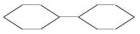 | D. | 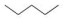 |
分析 有机物中一氯取代物的同分异构体取决于氢原子的种类,根据等效氢原子的判断方法来回答.
解答 解:A. 中含有4种氢原子,所以一氯取代物有4种;
中含有4种氢原子,所以一氯取代物有4种;
B. 中含有4种氢原子,所以一氯取代物有4种;
中含有4种氢原子,所以一氯取代物有4种;
C. 中含有4种氢原子,所以一氯取代物有4种;
中含有4种氢原子,所以一氯取代物有4种;
D. 中含有3种氢原子,所以一氯取代物有3种;
中含有3种氢原子,所以一氯取代物有3种;
故选D.
点评 本题考查同分异构体的书写,比较基础,注意利用等效氢进行的判断.

练习册系列答案
相关题目
20.化学与社会、生活密切相关.下列说法正确的是( )
| A. | 为加快漂粉精的漂白速率,使用时可滴加几滴醋酸 | |
| B. | 用作荧光灯内壁保护层的氧化铝纳米材料属于胶体 | |
| C. | “玉兔号”月球车太阳能电池帆板的材料是二氧化硅 | |
| D. | 海水中提溴的过程不涉及氧化还原反应 |
11.二氧化氯被国际上公认为安全、无毒的绿色消毒剂,以KClO3溶液为原料,采用电解法生产二氧化氯反应原理如下:4ClO3-+2H2O$\frac{\underline{\;通电\;}}{\;}$4ClO2↑+O2↑+4OH-.下列说法正确的是( )
| A. | 电解过程中OH-向阴极迁移 | |
| B. | 阳极反应式为:4OH--4e-=O2↑+2H2O | |
| C. | 毎有l mol电子转移,生成标准状况下5.6L气体 | |
| D. | 电解过程中阴极区溶液的pH降低 |
8.某溶液中可能含有下列5种离子中的某几种:Cl-、SO42-、SO32-、NH4+、Na+.为确认溶液组成进行如下实验:①向100mL上述溶液中加入足量BaCl2溶液,反应后将浊液过滤、洗涤、干燥,得沉淀4.50g,若向沉淀中加入过量的盐酸,仍有2.33g沉淀不溶.同时产生能使湿润红色石蕊试纸褪色的气体.②向①的滤液中加入足量的NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体0.56L(已换算成标准状况,假定产生的气体全部逸出).下列说法正确的是( )
| A. | 一定存在SO42-、SO32-、NH4+,可能存在Na+ | |
| B. | 一定存在SO42-、SO32-、NH4+,一定不存在Cl-、Na+ | |
| C. | 溶液中可能含有Cl-,且Na+浓度至少为0.15mol•L-1 | |
| D. | c(SO42-)=0.1mol•L-1,c(NH4+)<c(SO42-) |
5.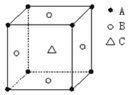 某物质的晶体中,含A、B、C三种元素,其排列方式如图所示(其中前后两面心上的B原子不能画出),晶体中A、B、C的原子个数比依次为( )
某物质的晶体中,含A、B、C三种元素,其排列方式如图所示(其中前后两面心上的B原子不能画出),晶体中A、B、C的原子个数比依次为( )
 某物质的晶体中,含A、B、C三种元素,其排列方式如图所示(其中前后两面心上的B原子不能画出),晶体中A、B、C的原子个数比依次为( )
某物质的晶体中,含A、B、C三种元素,其排列方式如图所示(其中前后两面心上的B原子不能画出),晶体中A、B、C的原子个数比依次为( )| A. | 1:2:1 | B. | 1:3:1 | C. | 2:2:1 | D. | 1:3:3 |
12.X、Y、Z、W、R属于短周期主族元素.X的原子半径在短周期主族元素中最大,Y核素的最外层电子数为m,次外层电子数为n,Z原子的L层电子数为m+n,M层电子数为m-n≠0,W与Z同主族,R与Y的核外电子数之比为2:1,下列叙述错误的是( )
| A. | Y的氢化物比R的氢化物稳定,沸点高 | |
| B. | Y分别与Z、W、R以两种元素组成的常见化合物有6种 | |
| C. | X与Y形成的两种常见化合物中阴、阳离子的个数比均为l:2 | |
| D. | Z、W、R最高价氧化物对应水化物的酸性由强到弱顺序是:R>W>Z |
9.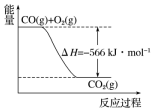 已知:
已知:
2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ•mol-1
根据以上热化学方程式和图象判断,下列说法正确的是( )
 已知:
已知:2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ•mol-1
根据以上热化学方程式和图象判断,下列说法正确的是( )
| A. | CO的燃烧热为283kJ | |
| B. | 图可表示由1molCO生成CO2的反应过程和能量关系 | |
| C. | 2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H>-452 kJ•mol-1 | |
| D. | 根据以上热化学方程式无法求算Na2O2(s)+CO(g)═Na2CO3 (s) 的反应热 |
10. 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料.有关说法正确的是( )
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料.有关说法正确的是( )
 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料.有关说法正确的是( )
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料.有关说法正确的是( )| A. | 合金的熔点通常比组分金属高,硬度比组分金属小 | |
| B. | 已知Ga处于ⅢA主族,可推知氮化镓化学式为Ga3N2 | |
| C. | 用金属铝与V2O5反应冶炼钒,铝作还原剂 | |
| D. | V原子序数为23,该原子的价电子构型为4S24P1 |
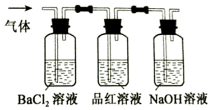 FeSO4受热分解的化学方程式为:2FeSO4$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+SO2↑+SO3↑
FeSO4受热分解的化学方程式为:2FeSO4$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+SO2↑+SO3↑