题目内容
4.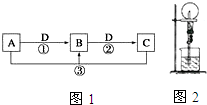 已知A、B、C、D 是中学化学的常见物质.且A、B、C 均含有同一种元索.在一定条件下它们之间的相气转化关系如图1所示(部分反应中的H2O已略去).
已知A、B、C、D 是中学化学的常见物质.且A、B、C 均含有同一种元索.在一定条件下它们之间的相气转化关系如图1所示(部分反应中的H2O已略去).请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,下列说法正确的是B•
A.C可由A、D直接化合得到
B.将少量碳酸钠粉末加入到新制A溶液中,pH 增大
C.MnO2与浓盐酸反应,若MnO2过量,浓盐酸可全部被消耗
D.1.2molA气体与1.5molD的碘化物溶液反应,D元素被部分氧化
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一.
①用蘸有浓盐酸的玻璃棒靠近运输A气体管道,若发生泄漏,则看到的现象是有白烟.
②反应①的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
③A气体可做喷泉实验,如图2引发喷泉实验的操作挤出胶头滴管中的水,打开止水夹.
(3)若D是氯碱工业的主要产品之一,B中的金属元素是地壳中含里最多的金属:
①则反应②的离子方程式是Al(OH)3+OH-=AlO2-+2H2O
②工业上向C溶液中通入CO2气体(填化学式),可制得B.
(4)若A、C、D都是常见气体.C是导致酸雨的主要气体.
①实验室需要清洗B,可选用CS2或热碱溶液
②提出一点关于大气污染的防治措施建议大力发展清洁能源、改进燃烧技术、工业废气处理、汽车尾气处理等.
分析 (1)若A可用于自来水消毒,应为Cl2,D是生产、生活中用量最大、用途最广的金属单质,应为Fe,则B为FeCl3,C为FeCl2;
(2)若A是一种碱性气体,常用作制冷剂,应为NH3,B是汽车尾气之一,遇空气会变色,应为NO,D为氧气;
(3)若D是氯碱工业的主要产品,B中的金属元素是地壳中含里最多的金属即为铝元素,则B为Al(OH)3,由转化关系可知,D为NaOH,C为NaAlO2;
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,应为SO2,则A为H2S,D为O2,B为S,据此答题.
解答 解:(1)若A可用于自来水消毒,应为Cl2,D是生产、生活中用量最大、用途最广的金属单质,应为Fe,则B为FeCl3,C为FeCl2,
A.氯气和铁直接化合得到的是氯化铁,故A错误;
B.将少量碳酸钠粉末加入到新制氯水中,碳酸钠与溶液中的盐酸反应,使pH 增大,故B正确;
C.MnO2与稀盐酸不反应,所以若MnO2过量,浓盐酸也不可全部被消耗,故C错误;
D.1.2mol氯气与1.5mol碘化亚铁溶液反应,铁元素不能被氧化,故D错误,
故选B;
(2)若A是一种碱性气体,常用作制冷剂,应为NH3,B是汽车尾气之一,遇空气会变色,应为NO,D为氧气,
①用蘸有浓盐酸的玻璃棒靠近运输A气体管道,若发生泄漏,则看到的现象是有白烟,故答案为:有白烟;
②反应①的化学方程式为 4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
③氨气可做喷泉实验,如图2引发喷泉实验的操作为挤出胶头滴管中的水,打开止水夹,
故答案为:挤出胶头滴管中的水,打开止水夹挤出胶头滴管中的水,打开止水夹;
(3)若D是氯碱工业的主要产品,B中的金属元素是地壳中含里最多的金属即为铝元素,则B为Al(OH)3,由转化关系可知,D为NaOH,C为NaAlO2,
①反应②的离子方程式是Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
②工业上向NaAlO2溶液中通入 CO2气体,可制得Al(OH)3,
故答案为:CO2;
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,应为SO2,则A为H2S,D为O2,B为S,据此答题;
①实验室需要清洗S,可选用CS2或热碱溶液,
故答案为:CS2或热碱溶液;
②关于大气污染的防治措施建议为大力发展清洁能源、改进燃烧技术、工业废气处理、汽车尾气处理等,
故答案为:大力发展清洁能源、改进燃烧技术、工业废气处理、汽车尾气处理等.
点评 本题考查无机物推断,属于开放性题目,具有一定难度,需要学生熟练掌握元素化合物性质.

| A. | 所有单键均有σ键 | B. | 双键、三键中必有σ键与π键 | ||
| C. | σ键、π键都可以绕轴自由旋转 | D. | π键不如σ键牢固 |
 和
和 代表不同元素的原子.
代表不同元素的原子.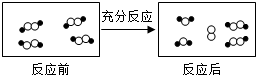
关于此反应说法错误的是( )
| A. | 一定属于吸热反应 | B. | 一定属于可逆反应 | ||
| C. | 一定属于氧化还原反应 | D. | 一定属于分解反应 |
| A. | 活性炭 | B. | 氯气 | C. | 次氯酸溶液 | D. | 二氧化碳 |
| A. | 14C与14N | B. | D2与H2 | C. | O2与O3 | D. | 35Cl与37Cl |
| A. | 铝是一种既可以与强酸反应又可以与强碱反应的金属 | |
| B. | 氧化铝按组成划分属于金属氧化物,按性质划分属于碱性氧化物 | |
| C. | 氢氧化铝具有较高的熔点和沸点,常用于制造耐火材料 | |
| D. | 铝是地壳中含量最多的元素,铝土矿是铝元素在地壳中的主要存在形式之一 |
| A. | 质子数为18 | B. | 中子数为40 | C. | 质量数为58 | D. | 核外电子数为22 |
