题目内容
14.某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为氯气与氨气反应的装置.
请回答下列问题:
(1)B装置的名称是干燥管;
(2)装置A的烧瓶中可装试剂碱石灰或生石灰等;
(3)装置F中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
E装置的作用是除去氯气中的氯化氢;
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出反应的化学方程式:3Cl2+8NH3═N2+6NH4Cl.
(5)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?在G连接导管直接通入盛有烧碱的烧杯中.
分析 (1)依据仪器形状说出其名称;
(2)碱石灰具有吸水性,利用碱石灰与浓氨水可制取氨气;
(3)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水;浓盐酸易挥发,制取的氯气中含有氯化氢,饱和食盐水可以除去氯气中的氯化氢杂质;
(4)氨气和氯气反应生成氯化铵和氮气;
(5)根据氯气的性质来确定尾气处理的方法.
解答 解:(1)依据仪器形状可知:B装置的名称是干燥管;
故答案为:干燥管;
(2)碱石灰或生石灰等与浓氨水混合可制取氨气,所以装置A的烧瓶中可装试剂为碱石灰或生石灰等;
故答案为:碱石灰或生石灰等;
(3)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水,化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;浓盐酸易挥发,制取的氯气中含有氯化氢,饱和食盐水可以除去氯气中的氯化氢杂质;
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;除去氯气中的氯化氢;
(4)氨气和氯气反应生成白烟氯化铵和空气的主要成分之一氮气,方程式:8NH3+3Cl2═6NH4Cl+N2;
故答案为:3Cl2+8NH3═N2+6NH4Cl;
(5)氯气是酸性气体,可以用氢氧化钠来进行尾气处理,或者是通入装有碱石灰的干燥管或气球收集,G处接NaOH溶液的尾气处理装置;
故答案为:G处接NaOH溶液的尾气处理装置.
点评 本题考查学生实验室制取氯气、氨气的方法、干燥、性质等方面的知识,考查角度广,把握实验室制备氯气、氨气的反应原理及二种气体的是解题关键,题目难度中等.

练习册系列答案
相关题目
19.涂改液是一种使用率较高的文具,很多同学都喜欢使用涂改液.经实验证实涂改液中含有许多挥发性有害物质,吸入后易引起慢性中毒而头晕、头痛,严重者抽搐、呼吸困难,二氯甲烷就是其中的一种.下列有关说法中不正确的是( )
| A. | 涂改液危害人体健康、污染环境,中小学生最好不要使用或慎用涂改液 | |
| B. | 二氯甲烷沸点较低 | |
| C. | 二氯甲烷易溶于水,涂改液沾到手上时,用水很容易洗去 | |
| D. | 二氯甲烷为四面体的结构,不存在同分异构体 |
6.下列分子中,各原子均处于同一平面上的是( )
| A. | NH3 | B. | CCl4 | C. | H3O+ | D. | CH2O |
3.今有0.3mol/L K2SO4溶液200mL,0.2mol/L MgSO4溶液300mL和0.1mol/L Al2(SO4)3溶液200mL,这三种溶液中硫酸根离子浓度之比是( )
| A. | 1:1:1 | B. | 3:2:1 | C. | 3:2:3 | D. | 1:1:3 |
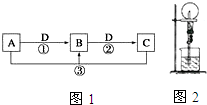 已知A、B、C、D 是中学化学的常见物质.且A、B、C 均含有同一种元索.在一定条件下它们之间的相气转化关系如图1所示(部分反应中的H2O已略去).
已知A、B、C、D 是中学化学的常见物质.且A、B、C 均含有同一种元索.在一定条件下它们之间的相气转化关系如图1所示(部分反应中的H2O已略去).