题目内容
19.以下互为同位素的是( )| A. | 14C与14N | B. | D2与H2 | C. | O2与O3 | D. | 35Cl与37Cl |
分析 质子数相同中子数不同的同一元素互称同位素,同一元素的不同单质互称同素异形体,据此分析解答.
解答 解:A.14C与14N质子数不同,是两种不同元素的原子,故A错误;
B.D2和H2是同一种单质,故B错误;
C.O2与O3是同一元素的不同单质,互称同素异形体,故C错误;
D.35Cl与37Cl是质子数相同中子数不同的同一元素,所以互称同位素,故D正确;
故选:D.
点评 本题考查的是同位素、同素异形体的判断,难度不大,侧重考查学生的辨别能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.有机物R是合成某药物的中间体,结构简式如图:

下列说法不正确的是( )

下列说法不正确的是( )
| A. | R分子有3种含氧官能团 | B. | 1molR最多消耗5mol NaOH | ||
| C. | R与氯化铁溶液发生显色反应 | D. | R能发生取代、加成、氧化 |
7.下列关于原子核外电子排布与元素在周期表中位置关系的表述中,正确的是( )
| A. | 原子的价电子排布为ns2np1~6的元素一定是主族元素 | |
| B. | 基态原子的p能级上有5个电子的元素一定是ⅦA族元素 | |
| C. | 原子的价电子排布为(n-1)d6~8ns2的元素一定位于ⅢB~ⅦB族 | |
| D. | 基态原子的N层上只有1个电子的元素一定是主族元素 |
11.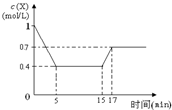 一定条件下,向密闭容器中加入1mol/L X发生反应:3X(g)?Y(g)+Z(g)△H<0,反应到5min时达到平衡,在15min时改变某一条件,到17min时又建立新平衡,X的物质的量浓度变化如图,下列说法中不正确的是( )
一定条件下,向密闭容器中加入1mol/L X发生反应:3X(g)?Y(g)+Z(g)△H<0,反应到5min时达到平衡,在15min时改变某一条件,到17min时又建立新平衡,X的物质的量浓度变化如图,下列说法中不正确的是( )
 一定条件下,向密闭容器中加入1mol/L X发生反应:3X(g)?Y(g)+Z(g)△H<0,反应到5min时达到平衡,在15min时改变某一条件,到17min时又建立新平衡,X的物质的量浓度变化如图,下列说法中不正确的是( )
一定条件下,向密闭容器中加入1mol/L X发生反应:3X(g)?Y(g)+Z(g)△H<0,反应到5min时达到平衡,在15min时改变某一条件,到17min时又建立新平衡,X的物质的量浓度变化如图,下列说法中不正确的是( )| A. | 0~5 min时,该反应的速率为v(X)=0.12 mol/(L•min) | |
| B. | 15 min时改变的条件可能是减小压强 | |
| C. | 15 min时改变的条件可能是升高温度 | |
| D. | 从初始到17 min时,X的转化率为30% |
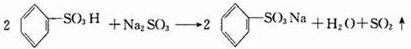 、③
、③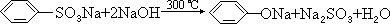 、④
、④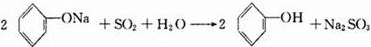 .
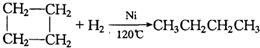
.
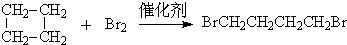 、
、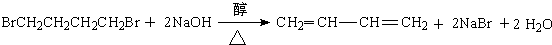 .
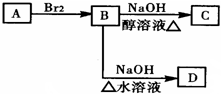
.
 ;C
;C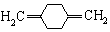 .
. .
.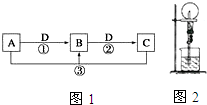 已知A、B、C、D 是中学化学的常见物质.且A、B、C 均含有同一种元索.在一定条件下它们之间的相气转化关系如图1所示(部分反应中的H2O已略去).
已知A、B、C、D 是中学化学的常见物质.且A、B、C 均含有同一种元索.在一定条件下它们之间的相气转化关系如图1所示(部分反应中的H2O已略去).