��Ŀ����
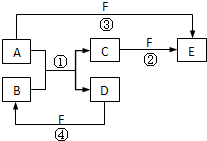 A��B��C��D��E��F�������ʵ��ת����ϵ��ͼ��ʾ����Ӧ����δ����������з�Ӧ�����û���Ӧ��
A��B��C��D��E��F�������ʵ��ת����ϵ��ͼ��ʾ����Ӧ����δ����������з�Ӧ�����û���Ӧ��
��1����A��D��F���Ƿǽ������ʣ���A��D����Ԫ��ͬ���壬A��F����Ԫ��ͬ���ڣ���Ӧ�ٵĻ�ѧ����ʽ�ǣ�______��
��2����A�dz����Ľ������ʣ�D��F����̬���ʣ���Ӧ����ˮ��Һ�н��У���Ӧ�ڣ���ˮ��Һ�н��У������ӷ���ʽ�ǣ�______����֪1g D��������F��Ӧ����Bʱ�ų�92.3kJ������д���÷�Ӧ���Ȼ�ѧ����ʽ��______��
��3����B��C��F������̬���ʣ���B�ж����ۺ͢�������Ӧ�ж���ˮ���ɣ���Ӧ����Ҫ�ŵ���ܷ�����A��D�����а������ɣ���C�ĵ���ʽ�ǣ�______����Ӧ�۵Ļ�ѧ����ʽ�ǣ�______��
��4����A��DΪ������Ԫ�ص��ʣ�������Ԫ�ص�ԭ������A��D��2��������Ԫ�ص�ԭ�Ӻ�������������D��A��2�����ۺ͢�������Ӧ�ж��к���ɫ�������ɣ�B�Ľṹʽ�ǣ�______����Ӧ�ܵĻ�ѧ����ʽ�ǣ�______��
�⣺��1��������Ԫ��ͬ����Ԫ��֮����û���Ӧ�ж��֣���Na��H2��O2��S��C��Si�ȣ���A��D��F���Ƿǽ������ʣ���A��D����Ԫ��ͬ���壬A��F����Ԫ��ͬ���ڣ���AΪC��DΪSi��FΪ
O2����Ӧ��ΪSiO2+2C Si+2CO�����ʴ�Ϊ��SiO2+2C
Si+2CO�����ʴ�Ϊ��SiO2+2C Si+2CO����
Si+2CO����
��2��A�dz����Ľ������ʣ�D��F����̬���ʣ��ɷ�Ӧ��ϵ��֪��AӦΪ��۽�������ӦΪFe��D��F����̬���ʣ�Ӧ�ֱ�ΪH2��Cl2��C����E�ķ�ӦΪ2Fe2++Cl2=2Fe3++2Cl-��
��Ӧ��H2+Cl2=2HCl����n��H2��=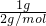 =0.5mol ʱ���ų�92.3kJ����������H2��g��+Cl2��g��=2HCl��g����H=-184.6KJ/moL��
=0.5mol ʱ���ų�92.3kJ����������H2��g��+Cl2��g��=2HCl��g����H=-184.6KJ/moL��
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��H2��g��+Cl2��g��=2HCl��g����H=-184.6KJ/moL��
��3����B��C��F������̬���ʣ���B�ж�����BΪCl2��ΪCl2��NH3�ķ�Ӧ������N2��HCl��N2�ĵ���ʽΪ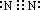 ��NH3��������Ӧ����NO��ˮ��Ϊ��ҵ������ķ�Ӧ����ѧ����ʽΪ
��NH3��������Ӧ����NO��ˮ��Ϊ��ҵ������ķ�Ӧ����ѧ����ʽΪ
4NH3+5O2 4NO+6H2O��
4NO+6H2O��
�ʴ�Ϊ��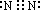 ��4NH3+5O2
��4NH3+5O2  4NO+6H2O��
4NO+6H2O��
��4����A��DΪ������Ԫ�ص��ʣ�������Ԫ�ص�ԭ������A��D��2��������Ԫ�ص�ԭ�Ӻ�������������D��A��2������AΪMg��DΪC��ΪMgO��C�ķ�Ӧ��CO2�ĽṹʽΪO=C=O���ۺ͢�������Ӧ�ж��к���ɫ�������ɣ���������ΪNO2����FΪHNO3����Ӧ��ΪC������ķ�Ӧ������ʽΪC+4HNO3��Ũ �� 4NO2��+CO2��+2H2O��
4NO2��+CO2��+2H2O��
����ʽΪC+4HNO3��Ũ �� 4NO2��+CO2��+2H20��
4NO2��+CO2��+2H20��
�ʴ�Ϊ��O=C=O��C+4HNO3��Ũ �� 4NO2��+CO2��+2H2O��
4NO2��+CO2��+2H2O��
��������1��������Ԫ��ͬ����Ԫ��֮����û���Ӧ�ж��֣���Na��H2��O2��S��C��Si�ȣ���A��D��F���Ƿǽ������ʣ���A��D����Ԫ��ͬ���壬A��F����Ԫ��ͬ���ڣ���AΪC��DΪSi��FΪ
O2���Դ˽��
��2��A�dz����Ľ������ʣ�D��F����̬���ʣ��ɷ�Ӧ��ϵ��֪��AӦΪ��۽�������ӦΪFe��D��F����̬���ʣ�Ӧ�ֱ�ΪH2��Cl2��
��3����B��C��F������̬���ʣ���B�ж�����BΪCl2��ΪCl2��NH3�ķ�Ӧ������N2��HCl��
��4����A��DΪ������Ԫ�ص��ʣ�������Ԫ�ص�ԭ������A��D��2��������Ԫ�ص�ԭ�Ӻ�������������D��A��2������AΪMg��DΪC��ΪMgO��C�ķ�Ӧ���ۺ͢�������Ӧ�ж��к���ɫ�������ɣ���������ΪNO2����FΪHNO3��
���������⿼��Ԫ�ػ�������ƶϣ���Ŀ��Ϣ�����ѶȽϴ���Ŀ�����ڳ���Ԫ�ػ���������ʺ���;������������ƶϣ�ѧϰ��ע�����֪ʶ�Ļ��ۣ�
O2����Ӧ��ΪSiO2+2C
 Si+2CO�����ʴ�Ϊ��SiO2+2C
Si+2CO�����ʴ�Ϊ��SiO2+2C Si+2CO����
Si+2CO������2��A�dz����Ľ������ʣ�D��F����̬���ʣ��ɷ�Ӧ��ϵ��֪��AӦΪ��۽�������ӦΪFe��D��F����̬���ʣ�Ӧ�ֱ�ΪH2��Cl2��C����E�ķ�ӦΪ2Fe2++Cl2=2Fe3++2Cl-��
��Ӧ��H2+Cl2=2HCl����n��H2��=
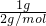 =0.5mol ʱ���ų�92.3kJ����������H2��g��+Cl2��g��=2HCl��g����H=-184.6KJ/moL��
=0.5mol ʱ���ų�92.3kJ����������H2��g��+Cl2��g��=2HCl��g����H=-184.6KJ/moL���ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��H2��g��+Cl2��g��=2HCl��g����H=-184.6KJ/moL��
��3����B��C��F������̬���ʣ���B�ж�����BΪCl2��ΪCl2��NH3�ķ�Ӧ������N2��HCl��N2�ĵ���ʽΪ
 ��NH3��������Ӧ����NO��ˮ��Ϊ��ҵ������ķ�Ӧ����ѧ����ʽΪ
��NH3��������Ӧ����NO��ˮ��Ϊ��ҵ������ķ�Ӧ����ѧ����ʽΪ4NH3+5O2
 4NO+6H2O��
4NO+6H2O���ʴ�Ϊ��
 ��4NH3+5O2
��4NH3+5O2  4NO+6H2O��
4NO+6H2O����4����A��DΪ������Ԫ�ص��ʣ�������Ԫ�ص�ԭ������A��D��2��������Ԫ�ص�ԭ�Ӻ�������������D��A��2������AΪMg��DΪC��ΪMgO��C�ķ�Ӧ��CO2�ĽṹʽΪO=C=O���ۺ͢�������Ӧ�ж��к���ɫ�������ɣ���������ΪNO2����FΪHNO3����Ӧ��ΪC������ķ�Ӧ������ʽΪC+4HNO3��Ũ ��
 4NO2��+CO2��+2H2O��
4NO2��+CO2��+2H2O������ʽΪC+4HNO3��Ũ ��
 4NO2��+CO2��+2H20��
4NO2��+CO2��+2H20���ʴ�Ϊ��O=C=O��C+4HNO3��Ũ ��
 4NO2��+CO2��+2H2O��
4NO2��+CO2��+2H2O����������1��������Ԫ��ͬ����Ԫ��֮����û���Ӧ�ж��֣���Na��H2��O2��S��C��Si�ȣ���A��D��F���Ƿǽ������ʣ���A��D����Ԫ��ͬ���壬A��F����Ԫ��ͬ���ڣ���AΪC��DΪSi��FΪ
O2���Դ˽��
��2��A�dz����Ľ������ʣ�D��F����̬���ʣ��ɷ�Ӧ��ϵ��֪��AӦΪ��۽�������ӦΪFe��D��F����̬���ʣ�Ӧ�ֱ�ΪH2��Cl2��
��3����B��C��F������̬���ʣ���B�ж�����BΪCl2��ΪCl2��NH3�ķ�Ӧ������N2��HCl��
��4����A��DΪ������Ԫ�ص��ʣ�������Ԫ�ص�ԭ������A��D��2��������Ԫ�ص�ԭ�Ӻ�������������D��A��2������AΪMg��DΪC��ΪMgO��C�ķ�Ӧ���ۺ͢�������Ӧ�ж��к���ɫ�������ɣ���������ΪNO2����FΪHNO3��
���������⿼��Ԫ�ػ�������ƶϣ���Ŀ��Ϣ�����ѶȽϴ���Ŀ�����ڳ���Ԫ�ػ���������ʺ���;������������ƶϣ�ѧϰ��ע�����֪ʶ�Ļ��ۣ�

��ϰ��ϵ�д�
�����Ŀ
 [��ѧ/ѡ��/���ʽṹ������]A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������Ԫ�ض�Ӧ�ĵ��ʾ�Ϊ���壮A��C��E��Ԫ�ص�ԭ�Ӻ����ֻ��2��δ�ɶԵ��ӣ�B��EԪ�ص�ԭ������֮�͵���C��DԪ�ص�ԭ������֮�ͣ�
[��ѧ/ѡ��/���ʽṹ������]A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������Ԫ�ض�Ӧ�ĵ��ʾ�Ϊ���壮A��C��E��Ԫ�ص�ԭ�Ӻ����ֻ��2��δ�ɶԵ��ӣ�B��EԪ�ص�ԭ������֮�͵���C��DԪ�ص�ԭ������֮�ͣ�