题目内容
16.下列说法正确的是( )| A. | 水的摩尔质量是18g | B. | 1分子硫酸的质量是98g | ||
| C. | 1molN2的质量是28g | D. | 摩尔是七个基本物理量之一 |
分析 A.摩尔质量的单位为g/mol;
B.结合n=$\frac{N}{{N}_{A}}$、m=nM计算;
C.结合m=nM计算;
D.摩尔为物质的量的单位,物质的量为七个基本物理量之一.
解答 解:A.水的摩尔质量是18g/mol,故A错误;
B.1分子硫酸的质量是$\frac{1}{{N}_{A}}$×98g/mol=$\frac{98}{{N}_{A}}$g,故B错误;
C.1molN2的质量是1mol×28g/mol=28g,故C正确;
D.物质的量为七个基本物理量之一,故D错误;
故选C.
点评 本题考查物质的量的计算,为高频考点,把握质量、物质的量、摩尔质量的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
19.化学与生产、生活、科学技术密切相关.下列有关说法错误的是( )
| A. | 发射神舟十一号飞船所用火箭的燃料是液氧和煤油,与用偏二甲肼和四氧化二氮作燃料相比,燃料毒性小、污染少 | |
| B. | 空气中氮氧化物不仅能产生光化学烟雾,还可能形成酸雨和破坏臭氧层 | |
| C. | 绿色食品并非指绿颜色的食品,而是指绿色植物或其加工的食品,不包括动物类食品 | |
| D. | 用肥皂水清洗蚊虫叮咬处时发生了化学变化 |
20.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 通常状况下,NA个N2所占的体积约为22.4L | |
| B. | 1L1mol•L-1NaOH水溶液中含有的氧原子数为NA | |
| C. | 足量Na与1molCl2完全反应,转移电子的数目为2NA | |
| D. | 1mol Na2O2中含有的阴离子数为2NA |
4.下列物质不属于硅酸盐产品的是( )
| A. | 青花瓷 | B. | 水泥 | C. | 石英 | D. | 玻璃 |
11.从海带中提取碘,需经过称量、灼烧、溶解、过滤、氧化、萃取和分液等操作,下列图示装置和原理能达到目的是( )
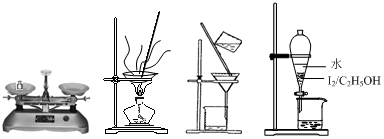

| A. | 称量 | B. | 灼烧 | C. | 过滤 | D. | 萃取 |
1.设NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
| A. | 1 mol NH4+ 所含质子数为10NA | |
| B. | 20 g氖气所含原子数约为6.02×1023 | |
| C. | 标准状况下,22.4 L SO2所含的分子数为NA | |
| D. | 常温常压下,32 g O2和O3的混合气体所含原子数为2NA |
5.化学实验设计和操作中必须十分重视安全和环境.下列实验问题处理方法正确的是( )
| A. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| B. | 在气体发生装置上直接点燃一氧化碳气体时,必须要先检验一氧化碳气体的纯度.最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声 | |
| C. | 制氧气时排水法收集氧气后出现倒吸现象,应立即松开试管上的橡皮塞 | |
| D. | 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |