题目内容
4.下列物质不属于硅酸盐产品的是( )| A. | 青花瓷 | B. | 水泥 | C. | 石英 | D. | 玻璃 |
分析 含有硅酸根离子的盐属于硅酸盐,传统硅酸盐产品包括:普通玻璃、陶瓷、水泥,据此解答.
解答 解:A.青花瓷主要成分是硅酸盐,属于硅酸盐材料,故A不选;
B.水泥主要成分是硅酸盐,属于硅酸盐材料,故B不选;
C.石英为二氧化硅,是氧化物不是硅酸盐,故C选;
D.玻璃主要成分是硅酸盐,属于硅酸盐材料,故D不选;
故选:C.
点评 本题考查无机非金属材料中的硅酸盐产品,熟悉硅酸盐的定义是解题关键,题目难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
7.已知充分燃烧a g乙炔(C2H2)气体时生成2mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧热的热化学方程式正确的是( )
| A. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2b kJ/mol | |
| B. | C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(l)△H=-b kJ/mol | |
| C. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-4b kJ/mol | |
| D. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=b kJ/mol |
8.电力工业所需的钢制构件在镀锌前需要经过酸洗,其基本原理是用盐酸除去其表面的Fe2O3•2H2O及FeO等杂质.回收废酸同时生产含铁产品的流程如图:
已知:i.酸洗钢制构件后得到废酸的主要成分如表所示.
ii pH<4时,Fe2+不易被氧气氧化.
(1)酸洗钢制构件时发生反应的离子方程式:2H++FeO=Fe2++H2O、6H++Fe2O3•H2O+Fe═3Fe2++4H2O.
(2)过程II中,发生的主要反应:FeCl2(s)十H2SO4(aq)?FeSO4(s)+2HCl( aq).
①加入过量H2SO4的作用是抑制Fe2+水解:防止pH>4时,Fe2+被氧气氧化:同时提供H+利于HC1气体的逸出;提供SO42-利于FeSO4固体析出(至少写出两点).
②用化学平衡原理解释鼓入空气的目的:空气带走HCl气体,促进平衡FeCl2(s)+H 2SO4(aq)?FeSO4(s)+2HCl(aq)向正反应方向移动,有利于FeSO4固体的析出.
(3)过程III中,FeSO4隔绝空气焙烧得到的尾气中含有两种可用于生产硫酸的氧化物,此过程发生反应的化学方程式是2FeSO4$\frac{\underline{\;焙烧\;}}{\;}$Fe2O3+SO2↑+SO3↑.
(4)过程IV发生反应的离子方程式是2Fe2++H2O2+8Cl-+2H+═2FeCl4-+2H2O.
(5)过程V:阴离子交换树脂可将FeCl4-选择性吸附分离,其过程可表示为ROH+X- $?_{脱附}^{吸附}$RX+OH-.当树脂吸附饱和后可直接用水洗涤树脂进行脱附,同时脱附过程发生反应:FeCl4-?Fe3++4C1-.
①吸附后溶液酸性下降的原因是利用阴离于空换树脂进行吸附时,树脂上的OH-被交换下来进入吸附后溶液.
②洗脱液中主要含有的溶质是FeCl3和HC1.

已知:i.酸洗钢制构件后得到废酸的主要成分如表所示.
| 成分 | Cl- | 游离HCl | Fe2+ | Fe3+ |
| 含量g•/L-1 | 130-160 | 50-70 | 60-80 | 0 |
(1)酸洗钢制构件时发生反应的离子方程式:2H++FeO=Fe2++H2O、6H++Fe2O3•H2O+Fe═3Fe2++4H2O.
(2)过程II中,发生的主要反应:FeCl2(s)十H2SO4(aq)?FeSO4(s)+2HCl( aq).
①加入过量H2SO4的作用是抑制Fe2+水解:防止pH>4时,Fe2+被氧气氧化:同时提供H+利于HC1气体的逸出;提供SO42-利于FeSO4固体析出(至少写出两点).
②用化学平衡原理解释鼓入空气的目的:空气带走HCl气体,促进平衡FeCl2(s)+H 2SO4(aq)?FeSO4(s)+2HCl(aq)向正反应方向移动,有利于FeSO4固体的析出.
(3)过程III中,FeSO4隔绝空气焙烧得到的尾气中含有两种可用于生产硫酸的氧化物,此过程发生反应的化学方程式是2FeSO4$\frac{\underline{\;焙烧\;}}{\;}$Fe2O3+SO2↑+SO3↑.
(4)过程IV发生反应的离子方程式是2Fe2++H2O2+8Cl-+2H+═2FeCl4-+2H2O.
(5)过程V:阴离子交换树脂可将FeCl4-选择性吸附分离,其过程可表示为ROH+X- $?_{脱附}^{吸附}$RX+OH-.当树脂吸附饱和后可直接用水洗涤树脂进行脱附,同时脱附过程发生反应:FeCl4-?Fe3++4C1-.
①吸附后溶液酸性下降的原因是利用阴离于空换树脂进行吸附时,树脂上的OH-被交换下来进入吸附后溶液.
②洗脱液中主要含有的溶质是FeCl3和HC1.
5.氮是地球上含量丰富的一种元素,“固氮”在工农业生产中有着重要作用,是几百年来科学家一直研究的课题.表列举了不同温度下大气固氮和工业固氮的部分K值.
(1)①分析数据可知:大气固氮反应属于吸热(填“吸热”或“放热”)反应.
②在一定温度下,将一定足的N2和O2通入到体积为1L的密闭容器中,当“大气固氮”反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是b.
a.增大压强 b.增大反应物的浓度 c.使用催化剂 d.升高温度
③从分子结构角度解释“大气固氮”和“工业固氮”反应的活化能都很高的原因:氮气分子中N≡N键能很大,断开N≡N需要吸收较高能量.
(2)分析表格数据可知“大气固氮”的反应正向进行的程度小,不适合大规模生产,故世界各国均采用合成氨的方法进行工业固氮.
①从平衡移动角度考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因从反应速率角度考虑,高温更好,但从催化剂活性等综合因素考虑选择500℃左右合适.
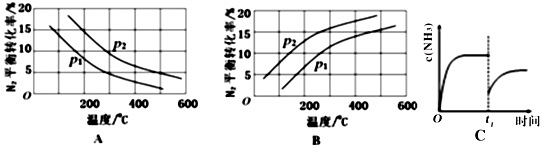
②将0.1molN2和0.1molH2通入一容积可变的容器中进行工业固氮反应,则下图所示N2的平衡转化率在不同压强(P1,P2)下随温度变化的曲线正确的是A(填“A”或“B”);比较P1、P2的大小关系 р2>р1;若300℃、压强P2时达到平衡,容器容积恰为100L,则此状态下反应的平衡常数K=1.3×l05 (计算结果保留2位有效数字).
③合成氨反应达到平衡后,t1时刻氮气浓度欲发生图C变化可采取的措施是容器容积不变条件下移走适量氨气,降低氨气的浓度.
(3)近年近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,
反应原理为:2N2(g)+6H2O(l)?4NH3(g)+3O2(g),则其反应热△H=+1530 kJ•mol-1.
(已知:
N2(g)+3H2(g)?2NH3(g)△H1=-92.4kJ•mol-1
2H2(g)+O2(g)?2H2O(l)△H2=-571.6kJ•mol-1 )
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×10-8 | 2×104 | 7×103 |
②在一定温度下,将一定足的N2和O2通入到体积为1L的密闭容器中,当“大气固氮”反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是b.
a.增大压强 b.增大反应物的浓度 c.使用催化剂 d.升高温度
③从分子结构角度解释“大气固氮”和“工业固氮”反应的活化能都很高的原因:氮气分子中N≡N键能很大,断开N≡N需要吸收较高能量.
(2)分析表格数据可知“大气固氮”的反应正向进行的程度小,不适合大规模生产,故世界各国均采用合成氨的方法进行工业固氮.
①从平衡移动角度考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因从反应速率角度考虑,高温更好,但从催化剂活性等综合因素考虑选择500℃左右合适.

②将0.1molN2和0.1molH2通入一容积可变的容器中进行工业固氮反应,则下图所示N2的平衡转化率在不同压强(P1,P2)下随温度变化的曲线正确的是A(填“A”或“B”);比较P1、P2的大小关系 р2>р1;若300℃、压强P2时达到平衡,容器容积恰为100L,则此状态下反应的平衡常数K=1.3×l05 (计算结果保留2位有效数字).
③合成氨反应达到平衡后,t1时刻氮气浓度欲发生图C变化可采取的措施是容器容积不变条件下移走适量氨气,降低氨气的浓度.
(3)近年近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,
反应原理为:2N2(g)+6H2O(l)?4NH3(g)+3O2(g),则其反应热△H=+1530 kJ•mol-1.
(已知:
N2(g)+3H2(g)?2NH3(g)△H1=-92.4kJ•mol-1
2H2(g)+O2(g)?2H2O(l)△H2=-571.6kJ•mol-1 )
12.NA表示阿伏加德罗常数数值,下列有关说法正确的是( )
| A. | 18.4 mol/L的浓硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol/L | |
| B. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| C. | 50 mL 14.0 mol•L-1浓硝酸与足量铜反应,转移的电子数为0.35 NA | |
| D. | 同温同压同体积下的两种气体12C18O和14N2具有的电子数相等 |
16.下列说法正确的是( )
| A. | 水的摩尔质量是18g | B. | 1分子硫酸的质量是98g | ||
| C. | 1molN2的质量是28g | D. | 摩尔是七个基本物理量之一 |
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| B. | 标准状况下,22.4L的CCl4中含有CCl4分子数目为NA | |
| C. | 25℃时,1L 1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| D. | 6.4gCu与一定浓度的HNO3完全反应得到混合气体,转移的电子数目为0.2NA |
14.在c(NaOH)=2c(NaAlO2)的溶液中滴加稀HCl,下列离子方程式正确的是( )
| A. | OH-+AlO2-+2H+=Al(OH)3 | B. | OH-+AlO2-+5H+=Al3++3H2O | ||
| C. | 2OH-+AlO2-+3H+=Al(OH)3+H2O | D. | OH-+2AlO2-+3H++H2O=2Al(OH)3 |