题目内容
9.将蔗糖用少量水湿润,然后在不断搅拌下加入浓硫酸,可看到蔗糖颜色变黑,体积逐渐膨胀,最后变成多孔的疏松固体,且产生刺激性气味的气体,上述过程中( )| A. | 体现浓硫酸的吸水性 | |
| B. | 体现了浓硫酸的脱水性 | |
| C. | 体现了浓硫酸的吸水性和脱水性 | |
| D. | 体现了浓硫酸的吸水性、脱水性和强氧化性 |
分析 浓硫酸能将有机物中H、O元素以2:1水的形式脱去而体现脱水性,能吸收水而具有吸水性,能和某些不活泼金属和非金属反应而体现强氧化性,由此分析解答.
解答 解:向蔗糖中加入浓硫酸时,蔗糖变黑,体积膨胀的这个过程中,浓硫酸将蔗糖中的H、O元素以2:1水的形式脱去而体现脱水性,生成的水被吸收而体现吸水性,将蔗糖氧化为C,体现浓硫酸的强氧化性,所以浓硫酸显示出吸水性、脱水性和强氧化性,故选D.
点评 本题考查浓硫酸的特性,明确元素化合物的性质特别是物质的特殊性质是解本题关键,注意能使有机物中的氢与氧以水的组成脱去以及与非金属单质的反应.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
17.(Ⅰ)部分弱酸的电离平衡常数如表:
(1)室温下①0.1mol•L-1 HCOONa,②0.1mol•L-1 NaClO,③0.1mol•L-1 Na2CO3,④0.1mol•L-1 NaHCO3溶液的pH由大到小的关系为③②④①.
(2)浓度均为0.1mol•L-1的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-).
(3)少量CO2通入到过量的NaClO溶液中发生反应的离子方程式ClO-+CO2+H2O=HCO3-+HClO.
(4)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(HCOO-)>c(Na+)>c(H+)>c(OH-).
(Ⅱ)某小组运用工业上离子交换膜法制烧碱的原理,用如图所示装置电解K2SO4溶液.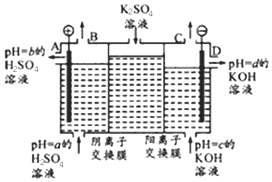
①该电解槽中通过阴离子交换膜的离子数<(填“>”“<”或“一”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为b<a<c<d;
③电解一段时间后,B出口与C出口产生气体的质量比为8:1.
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka=1.77 ×10-4 | Ka=4.0 ×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(2)浓度均为0.1mol•L-1的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-).
(3)少量CO2通入到过量的NaClO溶液中发生反应的离子方程式ClO-+CO2+H2O=HCO3-+HClO.
(4)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(HCOO-)>c(Na+)>c(H+)>c(OH-).
(Ⅱ)某小组运用工业上离子交换膜法制烧碱的原理,用如图所示装置电解K2SO4溶液.

①该电解槽中通过阴离子交换膜的离子数<(填“>”“<”或“一”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为b<a<c<d;
③电解一段时间后,B出口与C出口产生气体的质量比为8:1.
4.下列实验现象描述正确的是( )
| A. | 红热的铜丝在硫蒸汽中燃烧,产生黑色固体 | |
| B. | 碘水中加入少量CCl4,振荡静置后,下层颜色变浅,上层颜色变为紫色 | |
| C. | 往溴水中加入碘化钠溶液,溴水变为无色 | |
| D. | 氢气在Cl2中燃烧产生白色的烟 |
14.下列各组物质气化或熔化时,所克服的微粒间的作用力,属同种类型的是( )
| A. | 碘和干冰的升华 | B. | 二氧化硅和生石灰的熔化 | ||
| C. | 氯化钠和铁的熔化 | D. | 金刚石和氯化钾的熔化 |
1.加入Al能产生H2的溶液中一定能大量共存的是( )
| A. | K+、Na+、Br-、SO42- | B. | Na+、Ba2+、ClO-、Cl- | ||
| C. | Ca2+、Cl-、HCO3-、K+ | D. | NH4+、K+、OH-、SO42- |
18.为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 乙烷(乙烯) | 溴的四氯化碳溶液 | 洗气 |
| B | 硝基苯(硝酸) | H2O | 过滤 |
| C | 溴苯(溴) | NaOH溶液 | 分液 |
| D | 乙烯(SO2) | NaOH溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
19.如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.说法正确的是( )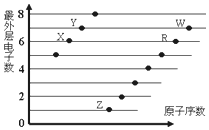

| A. | X与W形成的化合物中只有共价键 | B. | X与Z形成的化合物中只有离子键 | ||
| C. | 元素的非金属性:X>R>W | D. | 简单离子的半径:W>R>X |