题目内容
现有含NaCl、Na2SO4、Na2CO3和NaHCO3的固体混合物.某同学为测定其中各组分的含量,取部分样品溶于水,并设计了如下实验流程(所加试剂均为过量,反应①~③均为复分解反应).

请回答:
(1)气体W的化学式是 .
(2)溶液A中主要存在的微粒除了Na+、SO42-、Cl-之外还有 .
(3)反应②和③之后均需进行的操作的名称是 .
(4)试剂Y是 (填化学式).
(5)测定各组分的含量,需要测的数据有:混合物总质量、白色沉淀Ⅰ和Ⅱ分别的质量和 .

请回答:
(1)气体W的化学式是
(2)溶液A中主要存在的微粒除了Na+、SO42-、Cl-之外还有
(3)反应②和③之后均需进行的操作的名称是
(4)试剂Y是
(5)测定各组分的含量,需要测的数据有:混合物总质量、白色沉淀Ⅰ和Ⅱ分别的质量和
考点:常见阴离子的检验,常见阳离子的检验
专题:
分析:NaCl、Na2SO4、Na2CO3和NaHCO3的固体混合物中加入稀硝酸,反应生成的气体为二氧化碳气体,故W为二氧化碳;溶液A中含有Na+、SO42-、Cl-和加入的硝酸,故还含有H+、NO3-,分离固体和液体采用的方法是过滤,加入试剂Y是硝酸钡,若先加入AgNO3,则会同时生成Ag2SO4和AgCl沉淀,则应先加入过量的BaCl2[或Ba(NO3)2],生成BaSO4沉淀,然后在滤液中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,在所得滤液中加入过量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,最后所得溶液为NaNO3和Na2CO3的混合物,加入稀HNO3,最后进行蒸发操作可得固体NaNO3,据此解答即可.
解答:
解:NaCl、Na2SO4、Na2CO3和NaHCO3的固体混合物中加入稀硝酸,反应生成的气体为二氧化碳气体,故W为二氧化碳;溶液A中含有Na+、SO42-、Cl-和加入的硝酸,故还含有H+、NO3-,分离固体和液体采用的方法是过滤,加入试剂Y是硝酸钡,若先加入AgNO3,则会同时生成Ag2SO4和AgCl沉淀,则应先加入过量的BaCl2[或Ba(NO3)2],生成BaSO4沉淀,然后在滤液中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,在所得滤液中加入过量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,最后所得溶液为NaNO3和Na2CO3的混合物,加入稀HNO3,最后进行蒸发操作可得固体NaNO3,
(1)依据分析可知:气体W是CO2,故答案为:CO2;
(2)溶液A中含有Na+、SO42-、Cl-和加入的硝酸,故还含有H+、NO3-,故答案为:H+、NO3-;
(3)分离固体和液体采用的方法是过滤,故答案为:过滤;
(4)依据分析可知,Y是Ba(NO3)2,故答案为:Ba(NO3)2;
(5)测定各组分的含量,需要测的数据有:混合物总质量、白色沉淀Ⅰ和Ⅱ分别的质量和气体W的体积(标准状况)(或气体W的质量),故答案为:气体W的体积(标准状况)(或气体W的质量).
(1)依据分析可知:气体W是CO2,故答案为:CO2;
(2)溶液A中含有Na+、SO42-、Cl-和加入的硝酸,故还含有H+、NO3-,故答案为:H+、NO3-;
(3)分离固体和液体采用的方法是过滤,故答案为:过滤;
(4)依据分析可知,Y是Ba(NO3)2,故答案为:Ba(NO3)2;
(5)测定各组分的含量,需要测的数据有:混合物总质量、白色沉淀Ⅰ和Ⅱ分别的质量和气体W的体积(标准状况)(或气体W的质量),故答案为:气体W的体积(标准状况)(或气体W的质量).
点评:本题主要考查的是混合物的检验与分离,涉及复分解反应、试剂的选择等,难度不大.

练习册系列答案
相关题目
下列关于氯的说法错误的是( )
| A、氯水、液氯中均含有Cl2分子,故两者均为黄绿色 | ||||
B、
| ||||
| C、Cl2可以使湿润的有色布条褪色,是因为Cl2有漂白性 | ||||
| D、氯水中分子由多到少的顺序是:H2O>Cl2>HClO |
实验室里不同化学试剂的保存方法不尽相同,①NaOH溶液 ②大理石 ③NaCl溶液 ④稀硝酸4种试剂通常各自存放在如下图所示的玻璃试剂瓶中.按照试剂瓶的顺序存放试剂序号正确的是( )


| A、①②③④ | B、②①④③ |
| C、②③④① | D、②①③④ |
实验是研究化学的基础,如图中所示的实验方法、装置或操作均正确的是( )
A、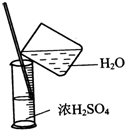 浓硫酸稀释 |
B、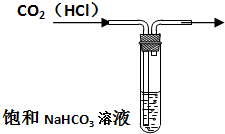 除去CO2中混有的杂质气体(HCl) |
C、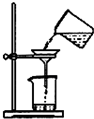 分离出AgNO3溶液中的AgCl |
D、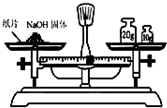 称量32.6g的NaOH固体 |
食品中加入营养强化剂是为了补充食品中缺乏的营养成分或微量元素.下列说法中不正确的是 ( )
| A、人体缺碘,可通过食用加碘盐补碘 |
| B、亚硝酸盐可常用作腌制肉类食品的防腐剂,大量进食易致癌 |
| C、维生素或钙、硒等不能添加在食品中 |
| D、缺铁性贫血,可通过食用铁强化酱油预防. |
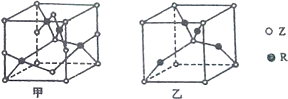 已知元素W、X、Y、Z、R为前四周期元素,且原子序数依次增大.元素W的负一价阴离子与某惰性气体结构相同,X是形成化合物种类最多的元素,Z原子L电子层上有2对成对电子,R+原子核外有3层电子且各层均处于全满状态.请回答下列问题:
已知元素W、X、Y、Z、R为前四周期元素,且原子序数依次增大.元素W的负一价阴离子与某惰性气体结构相同,X是形成化合物种类最多的元素,Z原子L电子层上有2对成对电子,R+原子核外有3层电子且各层均处于全满状态.请回答下列问题: