题目内容
 已知元素W、X、Y、Z、R为前四周期元素,且原子序数依次增大.元素W的负一价阴离子与某惰性气体结构相同,X是形成化合物种类最多的元素,Z原子L电子层上有2对成对电子,R+原子核外有3层电子且各层均处于全满状态.请回答下列问题:
已知元素W、X、Y、Z、R为前四周期元素,且原子序数依次增大.元素W的负一价阴离子与某惰性气体结构相同,X是形成化合物种类最多的元素,Z原子L电子层上有2对成对电子,R+原子核外有3层电子且各层均处于全满状态.请回答下列问题:(1)R+离子的外围电子排布式为
(2)上述五种元素,第一电离能最小的为
(3)元素X、Y、Z与W形成的最简单的化合物的沸点由小到大的顺序是
(4)与XYZ-互为等电子体微粒的化学式为
(5)R2+与NH3形成的配离子中所含的化学键类型为
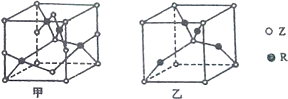
(6)已知Z、R能形成两种化合物,其晶胞如图所示,高温时,甲易转化为乙的原因为
考点:晶胞的计算,原子核外电子排布,判断简单分子或离子的构型,原子轨道杂化方式及杂化类型判断
专题:原子组成与结构专题,化学键与晶体结构
分析:元素W、X、Y、Z、R为前四周期元素,且原子序数依次增大,X是形成化合物种类最多的元素,则X为C元素;元素W的负一价阴离子与某惰性气体结构相同,则W为H元素;Z原子L电子层上有2对成对电子,则Z的电子排布式为1s22s22p4,Z为O元素,则Y为N元素;R+原子核外有3层电子且各层均处于全满状态,则R核外电子排布式为1s22s22p63s23p63d104s1,R为Cu元素,据此解答.
解答:
解:元素W、X、Y、Z、R为前四周期元素,且原子序数依次增大,X是形成化合物种类最多的元素,则X为C元素;元素W的负一价阴离子与某惰性气体结构相同,则W为H元素;Z原子L电子层上有2对成对电子,则Z的电子排布式为1s22s22p4,Z为O元素,则Y为N元素;R+原子核外有3层电子且各层均处于全满状态,则R原子核外电子排布式为1s22s22p63s23p63d104s1,R为Cu元素,
(1)R原子核外电子排布式为1s22s22p63s23p63d104s1,R+离子的外围电子排布式为1s22s22p63s23p63d10,相同轨道的电子能量相同,该基态原子有7种能量不同的电子,故答案为:1s22s22p63s23p63d10;7;
(2)同一主族元素的第一电离能随着原子序数的增大而减小,同一周期元素的第一电离能随着原子序数的增大而增大,故第一电离能最小的为O,故答案为:O;
(3)元素电负性越大,其氢化物的沸点越高,元素X、Y、Z与W形成的最简单的化合物的沸点由小到大的顺序是H2O>NH3>CH4,Y形成的简单氢化物为NH3,Z形成的简单氢化物为H2O,二者分子间能形成氢键,增大了氨的溶解度,故答案为:H2O>NH3>CH4;NH3与H2O分子间能形成氢键;
(4)CNO-电子数为22,等电子体为电子数相等,故与CNO-互为等电子体微粒的化学式CO2、N2O、SCN-等,CNO-的中心原子C电子对数=2+
=2,故杂化方式为SP杂化,NO3-中心原子N电子对数=3+
=3,孤电子对数为0,则空间构型是平面三角形,故答案为:CO2、N2O、SCN-等;SP;平面三角形;
(5)Cu2+与NH3形成的配离子中Cu2+与NH3之间的化学键为配位键,N-H为极性共价键,故答案为:配位键、极性键;
(6)已知O、Cu能形成晶胞如图所示的两种化合物,甲中黑色球(Cu)位于体心,其数目为4,白色球(O)位于晶胞棱、面心、体心和顶点,其数目为4×
+2×
+1+8×
=4,Cu、O原子数目之比为1:1,则甲的化学式为CuO,乙中黑色球(Cu)位于体心,其数目为4,白色球(O)位于体心和顶点,其数目为1+8×
=2,Cu与O原子个数之比为2:1,则乙的化学式为Cu2O,Cu2O中Cu原子d轨道为全满状态,比较稳定,故高温时甲易转化为乙,若甲晶体中一个晶胞的边长为apm,则甲晶体的密度为
=
=
g/cm3,
故答案为:Cu2O中Cu原子d轨道为全满状态,比较稳定;
.
(1)R原子核外电子排布式为1s22s22p63s23p63d104s1,R+离子的外围电子排布式为1s22s22p63s23p63d10,相同轨道的电子能量相同,该基态原子有7种能量不同的电子,故答案为:1s22s22p63s23p63d10;7;
(2)同一主族元素的第一电离能随着原子序数的增大而减小,同一周期元素的第一电离能随着原子序数的增大而增大,故第一电离能最小的为O,故答案为:O;
(3)元素电负性越大,其氢化物的沸点越高,元素X、Y、Z与W形成的最简单的化合物的沸点由小到大的顺序是H2O>NH3>CH4,Y形成的简单氢化物为NH3,Z形成的简单氢化物为H2O,二者分子间能形成氢键,增大了氨的溶解度,故答案为:H2O>NH3>CH4;NH3与H2O分子间能形成氢键;
(4)CNO-电子数为22,等电子体为电子数相等,故与CNO-互为等电子体微粒的化学式CO2、N2O、SCN-等,CNO-的中心原子C电子对数=2+
| 4+1-2-3 |
| 2 |
| 5+1-2×3 |
| 2 |
(5)Cu2+与NH3形成的配离子中Cu2+与NH3之间的化学键为配位键,N-H为极性共价键,故答案为:配位键、极性键;
(6)已知O、Cu能形成晶胞如图所示的两种化合物,甲中黑色球(Cu)位于体心,其数目为4,白色球(O)位于晶胞棱、面心、体心和顶点,其数目为4×
| 1 |
| 4 |
| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 8 |
| m |
| V |
| ||
| (a×10-10cm)3 |
| 3.2×1033 |
| a3NA |
故答案为:Cu2O中Cu原子d轨道为全满状态,比较稳定;
| 3.2×1033 |
| a3NA |
点评:本题综合查物质结构与性质,推断元素是解题的关键,涉及核外电子排布规律、配位键、杂化理论与分子结构、晶胞计算等,难度中等,掌握均摊法进行晶胞的有关计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
有关物质用途,用离子方程式解释不正确的是( )
| A、氢氟酸刻蚀玻璃:SiO2+4HF=SiF4↑+2H2O |
| B、明矾用于净水:Al3++3H2O=Al(OH)3+3H+ |
| C、纯碱去除油污:CO32-+H2O?HCO3-+OH- |
| D、氯气制备“84”消毒液:Cl2+2OH-=Cl-+ClO-+H2O |
已知HA为酸性略强于醋酸的一元弱酸,则在0.1mol?L-1 NaA溶液中,离子浓度关系正确的是( )
| A、c(Na+)>c(A-)>c(H+)>c(OH-) |
| B、c(Na+)+c(H+)=c(A-)+c(OH-) |
| C、c(Na+)+c(OH-)=c(A-)+c(H+) |
| D、c(Na+)>c(OH-)>c(A-)>c(H+) |
下列物质长久放置在空气中会发生相应的变化,其中发生了氧化还原反应的是( )
| A、浓硫酸的质量增加 |
| B、铝的表面生成致密的氧化物薄膜 |
| C、澄清的石灰水变浑浊 |
| D、氢氧化钠固体发生潮解 |
短周期主族元素X、Y、Z、W的原子序数依次增大.X与W同主族,X、W的单质在标准状况下的状态不同.Y是空气中含量最高的元素,Z原子最外层电子数是其内层电子总数的3倍,Z2-与W+具有相同的电子层结构.下列说法正确的是( )
| A、原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B、元素Y的简单气态氢化物的热稳定性比Z的强 |
| C、由X、Y、Z三种元素形成的化合物的水溶液可能呈碱性 |
| D、化合物X2Z2与W2Z2所含化学键类型完全相同 |
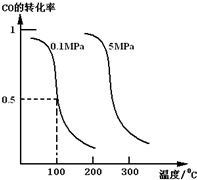 研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.在催化剂作用下,CO可用于合成甲醇:CO(g)+2H2(g)?CH3OH(g).
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.在催化剂作用下,CO可用于合成甲醇:CO(g)+2H2(g)?CH3OH(g).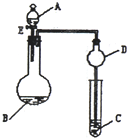 用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:
用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:
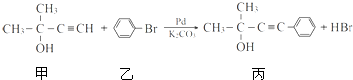
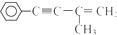 的反应条件是
的反应条件是