题目内容
下列实验方案中,不能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 验证Ksp(AgCl)>Ksp(AgI) | 向NaCl溶液中滴加AgNO3溶液,产生白色沉淀,再滴加KI溶液,可观察到白色沉淀转化为黄色沉淀 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置.可观察到下层液体呈紫色 |
| D | 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.向NaCl溶液中滴加AgNO3溶液,产生白色沉淀,再滴加KI溶液,可观察到白色沉淀转化为黄色沉淀,说明AgI较AgCl难溶;
B.硝酸能将亚铁离子氧化为铁离子而干扰实验;
C.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液,首先析出的金属,活动性较差.
B.硝酸能将亚铁离子氧化为铁离子而干扰实验;
C.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液,首先析出的金属,活动性较差.
解答:
解:A.白色沉淀转化为黄色沉淀,说明生成AgI,生成物溶度积更小,则Ksp(AgCl)>Ksp(AgI),故A正确;
B.加入稀硫酸后,酸性条件下,硝酸根离子具有强氧化性,能将亚铁离子氧化为铁离子而干扰实验,所以不能实现实验目的,故B错误;
C.将少量溴水加入KI溶液中,再加入CCl4,振荡,静置.可观察到下层液体呈紫色,说明二者发生氧化还原反应2I-+Br2=2Br-+I2,溴是氧化剂、碘是氧化产物,所以溴的氧化性大于碘,所以能实现实验目的,故C正确;
D.用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液,首先析出的金属,金属阳离子氧化性强,则对应的单质的还原性弱,活动性较差,故D正确.
故选B.
B.加入稀硫酸后,酸性条件下,硝酸根离子具有强氧化性,能将亚铁离子氧化为铁离子而干扰实验,所以不能实现实验目的,故B错误;
C.将少量溴水加入KI溶液中,再加入CCl4,振荡,静置.可观察到下层液体呈紫色,说明二者发生氧化还原反应2I-+Br2=2Br-+I2,溴是氧化剂、碘是氧化产物,所以溴的氧化性大于碘,所以能实现实验目的,故C正确;
D.用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液,首先析出的金属,金属阳离子氧化性强,则对应的单质的还原性弱,活动性较差,故D正确.
故选B.
点评:本题考查了实验方案评价,明确实验原理是解本题关键,根据物质的性质来分析解答,易错选项是B、D,注意硝酸根离子的性质,为易错点,难度中等.

练习册系列答案
相关题目
下列根据反应原理设计的应用,不正确的是( )
| A、CO32-+H2O?HCO3-+OH- Na2CO3与Al2(SO4)3溶液混合作灭火剂 |
| B、Al3++3H2O?Al(OH)3+3H+ 明矾净水 |
| C、TiCl4+(x+2)H2O(过量)?TiO2?xH2O↓+4HCl 制备TiO2纳米粉 |
| D、SnCl2+H2O?Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入浓盐酸 |
以下对核外电子运动状况的描述正确的是( )
| A、同一原子中,2p,3p,4p能级的轨道依次增多,均为哑铃状 |
B、当碳原子的核外电子排布由 转变为 转变为 时,这一过程中释放能量 时,这一过程中释放能量 |
| C、3p2表示3p能级有两个轨道 |
| D、在同一能级上运动的电子,其运动状态完全相同 |
取0.04mol KMnO4固体加热一段时间后,收集到a mol单质气体,在反应后的残留固体中加入过量的浓盐酸并加热,充分反应后又收集到b mol单质气体,假设最后锰元素全部以Mn2+存在于溶液中,则a+b的最小值为( )
| A、0.02 | B、0.04 |
| C、0.08 | D、0.1 |
将a g块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如图的实线所示.在相同的条件下,将b g(a>b)粉末状碳酸钙与同浓度盐酸反应,则相应的曲线(图中虚线所示)正确的是( )
A、 |
B、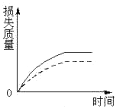 |
C、 |
D、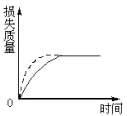 |
下列图示对应的化学实验的基本操作,其中装置合理、操作规范的是( )

| A、甲装置可用于除去碳酸钠固体中含有的少量碳酸氢钠 |
| B、乙装置可用于碳酸钙固体和氯化钠溶液的分离 |
| C、丙装置可用于分离出I2的CCl4溶液 |
| D、丁装置可用于酒精和水的分离 |
