题目内容
下列根据反应原理设计的应用,不正确的是( )
| A、CO32-+H2O?HCO3-+OH- Na2CO3与Al2(SO4)3溶液混合作灭火剂 |
| B、Al3++3H2O?Al(OH)3+3H+ 明矾净水 |
| C、TiCl4+(x+2)H2O(过量)?TiO2?xH2O↓+4HCl 制备TiO2纳米粉 |
| D、SnCl2+H2O?Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入浓盐酸 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:A、灭火剂是碳酸氢钠和硫酸铝混合生成二氧化碳;
B、明矾净水石铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用,可以净水;
C、制备TiO2纳米粉,利用水解反应生成沉淀制备;
D、配制氯化亚锡溶液时加入浓盐酸抑制水解;
B、明矾净水石铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用,可以净水;
C、制备TiO2纳米粉,利用水解反应生成沉淀制备;
D、配制氯化亚锡溶液时加入浓盐酸抑制水解;
解答:
解:A、灭火剂是碳酸氢钠和硫酸铝混合生成二氧化碳,3HCO3-+Al3+=Al(OH)3↓+3CO2↑,故A错误;
B、明矾净水是铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用,可以净水,Al3++3H2O?Al(OH)3+3H+,故B正确;
C、制备TiO2纳米粉,利用水解进行沉淀制备,故C正确;
D、配制氯化亚锡溶液时加入浓盐酸抑制水解,SnCl2+H2O?Sn(OH)Cl↓+HCl,故D正确;
故选A.
B、明矾净水是铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用,可以净水,Al3++3H2O?Al(OH)3+3H+,故B正确;
C、制备TiO2纳米粉,利用水解进行沉淀制备,故C正确;
D、配制氯化亚锡溶液时加入浓盐酸抑制水解,SnCl2+H2O?Sn(OH)Cl↓+HCl,故D正确;
故选A.
点评:本题考查了盐类水解的分析应用,注意一下因素的 分析判断,掌握基础是关键,题目较简单.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
已知I-、Fe2+、SO2、Cl-和H2O2均有还原性、它们在酸性溶液中还原性强弱顺序为Cl-<H2O2<Fe2+<I-<SO2,则下列反应不能发生的是( )
| A、2Fe2++I2=2Fe3++2I- |
| B、2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| C、SO2+I2+2H2O=H2SO4+2HI |
| D、H2O2+SO2=H2SO4 |
下列图象表达正确的是( )
A、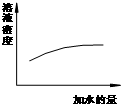 浓硫酸的稀释 |
B、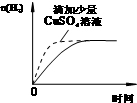 等量的盐酸与过量的锌粉反应 |
C、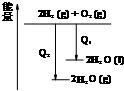 氢气与氧气反应中的能量变化 |
D、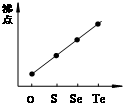 气态氢化物沸点 |
下列关于钢铁的析氢腐蚀的说法中正确的是( )
| A、铁为正极 |
| B、碳为正极 |
| C、溶液中氢离子浓度不变 |
| D、析氢腐蚀在任何溶液中都会发生 |
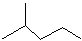 表示的分子式
表示的分子式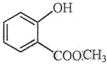 中的含氧官能团的名称为
中的含氧官能团的名称为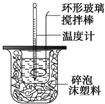 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下: