题目内容
将a g块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如图的实线所示.在相同的条件下,将b g(a>b)粉末状碳酸钙与同浓度盐酸反应,则相应的曲线(图中虚线所示)正确的是( )
A、 |
B、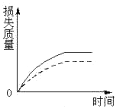 |
C、 |
D、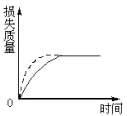 |
考点:化学反应速率的影响因素
专题:
分析:由题意可知,图中实线表示的块状的碳酸钙与足量的盐酸反应,虚线所示粉末状碳酸钙与同浓度的盐酸反应,利用接触面积对反应速率的影响来解答.
解答:
解:固体表面积越大,则反应速率越大,加入粉末状碳酸钙与同浓度盐酸反应,较块状碳酸钙反应速率大,
即相同时间内虚线所示的曲线对应的损失的质量大,因为 a>b导致最终损失的质量a>b,由图象可知,只有C符合,
故选C.
即相同时间内虚线所示的曲线对应的损失的质量大,因为 a>b导致最终损失的质量a>b,由图象可知,只有C符合,
故选C.
点评:本题考查影响化学反应速率的因素及图象分析,为高频考点,明确接触面积对反应速率的影响及盐酸足量时参加反应的碳酸钙的质量相同是解答本题的关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在15.2g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4g沉淀,则下列表示气体X组成的选项中合理的是( )
| A、0.3 mol NO2、0.1 mol NO |
| B、0.3 mol NO、0.1 mol NO2 |
| C、0.6 mol NO |
| D、0.3 mol NO2 |
下列说法正确的是( )
| A、100 mL3 mol?L-1的硫酸与100 mL H2O混合,硫酸物质的量浓度改变为1.5 mol?L-1 |
| B、把100 g 20%的NaCl溶液与100 g H2O混合后,NaCl溶液的质量分数是10% |
| C、把200 mL3 mol?L-1的BaCl2溶液与100 mL 3 mol?L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是3 mol?L-1 |
| D、把100 mL 20%的NaOH溶液与100 mL H2O混合后,NaOH溶液的质量分数是10% |