题目内容
按下列要求写出相应方程式
(1)NaHCO3溶于水电离方程式
(2)Al(OH)3电离方程式
(3)氯气与水反应离子方程式
(4)以Fe3O4为原料的铝热反应化学方程式
(5)甲烷(CH4)燃料电池,以铂作电极,KOH溶液为电解质溶液,其负极电极反应式为
(6)一种新型燃料电池,一极通入空气,另一极通入丁烷(C4H10)气体,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-,其负极电极反应式为 .
(1)NaHCO3溶于水电离方程式
(2)Al(OH)3电离方程式
(3)氯气与水反应离子方程式
(4)以Fe3O4为原料的铝热反应化学方程式
(5)甲烷(CH4)燃料电池,以铂作电极,KOH溶液为电解质溶液,其负极电极反应式为
(6)一种新型燃料电池,一极通入空气,另一极通入丁烷(C4H10)气体,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-,其负极电极反应式为
考点:电离方程式的书写,离子方程式的书写,电极反应和电池反应方程式
专题:
分析:(1)碳酸氢钠为强电解质完全电离出钠离子和碳酸氢根离子;
(2)氢氧化铝属于两性氢氧化物,有酸式电离和碱式电离两种电离方式;
(3)氯气与水反应生成氯化氢和次氯酸;
(4)四氧化三铁与铝反应生成铁和氧化铝;
(5)负极上甲烷发生氧化反应,生成碳酸根离子;
(6)燃料所在极为负极,负极失去电子发生氧化反应.
(2)氢氧化铝属于两性氢氧化物,有酸式电离和碱式电离两种电离方式;
(3)氯气与水反应生成氯化氢和次氯酸;
(4)四氧化三铁与铝反应生成铁和氧化铝;
(5)负极上甲烷发生氧化反应,生成碳酸根离子;
(6)燃料所在极为负极,负极失去电子发生氧化反应.
解答:
解:(1)NaHCO3溶于水电离方程式,:NaHCO3=Na++HCO3-;
故答案为:NaHCO3=Na++HCO3-;
(2)氢氧化铝属于两性氢氧化物,有酸式电离和碱式电离两种电离方式,电离方程式为:Al(OH)3? Al3++3OH-?Al(OH)3
Al3++3OH-?Al(OH)3  H++AlO2-+H2O;
H++AlO2-+H2O;
故答案为:Al(OH)3? Al3++3OH-;Al(OH)3
Al3++3OH-;Al(OH)3  H++AlO2-+H2O.
H++AlO2-+H2O.
(3)氯气与水反应生成氯化氢和次氯酸,离子方程式为:Cl2+H2O=H++Cl-+HClO;
故答案为:Cl2+H2O=H++Cl-+HClO;
(4)四氧化三铁与铝反应生成铁和氧化铝,化学方程式为:8Al+3Fe3O4
4Al2O3+9Fe;
故答案为:8Al+3Fe3O4
4Al2O3+9Fe;
(5)甲烷(CH4)燃料电池,以铂作电极,KOH溶液为电解质溶液,负极上甲烷发生氧化反应,生成碳酸根离子,电极反应式:CH4-8e-+10OH-=CO32-+7H2O;
故答案为:CH4-8e-+10OH-=CO32-+7H2O;
(6)该燃料电池中通入丁烷的一极为负极,发生氧化反应,电极反应式为:C4H10-26e-+13O2-=4CO2+5H2O;
故答案为:C4H10-26e-+13O2-=4CO2+5H2O.
故答案为:NaHCO3=Na++HCO3-;
(2)氢氧化铝属于两性氢氧化物,有酸式电离和碱式电离两种电离方式,电离方程式为:Al(OH)3?
 Al3++3OH-?Al(OH)3
Al3++3OH-?Al(OH)3  H++AlO2-+H2O;
H++AlO2-+H2O;故答案为:Al(OH)3?
 Al3++3OH-;Al(OH)3
Al3++3OH-;Al(OH)3  H++AlO2-+H2O.
H++AlO2-+H2O.(3)氯气与水反应生成氯化氢和次氯酸,离子方程式为:Cl2+H2O=H++Cl-+HClO;
故答案为:Cl2+H2O=H++Cl-+HClO;
(4)四氧化三铁与铝反应生成铁和氧化铝,化学方程式为:8Al+3Fe3O4
| ||
故答案为:8Al+3Fe3O4
| ||
(5)甲烷(CH4)燃料电池,以铂作电极,KOH溶液为电解质溶液,负极上甲烷发生氧化反应,生成碳酸根离子,电极反应式:CH4-8e-+10OH-=CO32-+7H2O;
故答案为:CH4-8e-+10OH-=CO32-+7H2O;
(6)该燃料电池中通入丁烷的一极为负极,发生氧化反应,电极反应式为:C4H10-26e-+13O2-=4CO2+5H2O;
故答案为:C4H10-26e-+13O2-=4CO2+5H2O.
点评:本题考查了离子方程式、电离方程式、化学方程式、电极反应式的书写,难点在于燃料电池电极反应式的书写,明确原电池工作原理是解题关键,题目难度不大.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
下列关于钢铁的析氢腐蚀的说法中正确的是( )
| A、铁为正极 |
| B、碳为正极 |
| C、溶液中氢离子浓度不变 |
| D、析氢腐蚀在任何溶液中都会发生 |
实验室制取氧气的试管上会有MnO2,最好用下列那种试剂除去( )
| A、稀盐酸 | B、热的浓盐酸 |
| C、水 | D、NaOH溶液 |
现有等物质的量组成的Fe、Cu合金共0.1mol,研成粉末后,全部投入稀硝酸中,微热使其充分反应,已知硝酸的还原产物只有NO.由于HNO3用量的不同,溶液中的金属离子和残留固体的成分会有多种情况.下列说法正确的是( )
| A、根据溶液中的金属离子和残留固体的成分最多会有5种情况 |
| B、若金属有剩余,在溶液中再滴入稀硫酸后,金属不会溶解 |
| C、当合金刚好溶解时,在标准状况下产生2.24LNO |
| D、若合金全部溶解,在溶液中加入过量的氨水,(已知铜离子可转化为四氨合铜络离子溶于水)则经过滤、洗涤、干燥、充分灼烧、称量可得固体4g |
实验室欲用氯化钠固体配制500mL、0.10mol?L-1的NaCl溶液,下列叙述正确的是( )
| A、实验用到的仪器有:托盘天平、烧杯、1000mL容量瓶、玻璃棒 |
| B、将称量好的固体放入500mL容量瓶中溶解 |
| C、定容时若俯视刻度,则所得溶液浓度偏高 |
| D、定容后翻转摇匀,发现液面下降,又加入蒸馏水到刻度线 |
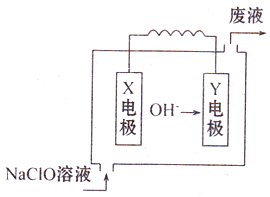 如图为Mg-NaClO燃料电池结构示意图.已知电解质溶液为NaOH溶液,且两电极中有一电极为石墨电极.
如图为Mg-NaClO燃料电池结构示意图.已知电解质溶液为NaOH溶液,且两电极中有一电极为石墨电极. 把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中,有0.58g白色沉淀析出,向所得的浊液中,逐滴加入0.5mol/L的盐酸,加入盐酸的体积和生成沉淀的质量如图所示.
把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中,有0.58g白色沉淀析出,向所得的浊液中,逐滴加入0.5mol/L的盐酸,加入盐酸的体积和生成沉淀的质量如图所示.