题目内容
11.化学与科学、技术、社会、环境密切相关.下列有关说法中不正确的是( )| A. | 工业上,用焦炭在电炉中还原二氧化硅得到含杂质的粗硅 | |
| B. | 煤经过气化和液化两个物理变化,可变为清洁能源 | |
| C. | 如将纳米材料分散到液体分散剂中,该分散系可发生丁达尔现象,由此可推测纳米材料的直径为1~100 nm之间 | |
| D. | 将苦卤浓缩、氧化,鼓入热空气或水蒸气提取海水中的溴,溴元素又称“海洋元素” |
分析 A.碳与二氧化硅反应生成一氧化碳和硅;
B.物理变化与化学变化本质区别是否有新物质生成;
C.依据胶体分散系中分散质粒度判断;
D.溴离子发生氧化反应生成溴单质,然后鼓入热空气或水蒸气提取海水中的溴.
解答 解:A.碳与二氧化硅反应生成一氧化碳和硅,工业上用此反应制取粗硅,故A正确;
B.煤的气化和液化过程中,有新物质生成,属于化学变化,故B错误;
C.胶体分散系中分散质粒度介于1-100nm,故C正确;
D.溴离子发生氧化反应生成溴单质,离子反应方程式为Cl2+2Br-=Br2+2Cl-,溴具有挥发性,然后鼓入热空气或水蒸气提取海水中的溴,故D正确;
故选:B.
点评 本题为综合题,考查了粗硅的制备、煤的综合利用、胶体的性质、海水提溴,掌握基础是解题关键,题目难度不大.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
1.NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2 L的甲醇所含的氢原子数大于2NA | |
| B. | 常温下,1mol•L-1的Na2CO3溶液中CO32-的个数必定小于NA | |
| C. | 1mol Cu与含2mol H2SO4,的浓硫酸充分反应,生成的S02的分子个数为NA | |
| D. | 1mol苯分子中含有3NA个碳碳双键 |
2.下列说法正确的是( )
| A. | 1 mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热 | |
| B. | 强酸和强碱的稀溶液发生中和反应一定是放热反应,弱酸和弱碱反应一定也是放热反应 | |
| C. | CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,故反应一定是吸热反应 | |
| D. | 酸和碱发生中和反应生成1 mol 水,这时的反应热叫中和热 |
19.12月3日9点左右,成绵高速出现浓雾导致多起交通事故,雾中小水滴直径范围是( )
| A. | 小于1nm | B. | 在1nm~100nm间 | C. | 大于100nm | D. | 无法确定 |
16.短周期元素X、Z、W、Q在元素周期表中的位置如图所示,其中X元素原子最外层电子数是最内层电子数的3倍,则下列说法正确的是( )
| X | Y | ||
| Z | W | Q |
| A. | X、W能与钠形成摩尔质量相同的化合物 | |
| B. | 含X和Z元素的常见化合物为分子晶体 | |
| C. | 最高价氧化物对应的水化物酸性:W>Q | |
| D. | 原子半径大小关系:Q>W>Z>Y |
3.下列化学用语书写正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 硝基苯的结构简式: | |
| C. | (CH3 CH2)2 CHCH2CH3 的名称:2-乙基丁烷 | |
| D. | 甲基的电子式为: |
1.下述实验不能达到预期目的是:
| 编号 | 实验内容 | 实验目的 |
| A | 用平行光照射 | 区别淀粉溶液和氯化钠溶液 |
| B | 加入CaCO3粉末,充分反应后过滤 | 除去CaCl2溶液中的FeCl3 |
| C | 通过灼烧的Cu粉末,收集气体 | 除去N2中的少量O2 |
| D | 滴入稀盐酸,同时用pH计测定至溶液呈中性 | 除去KNO3溶液中的KOH |
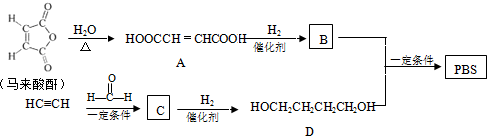
 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$
 →CH≡CH的化学方程式(注明条件)
→CH≡CH的化学方程式(注明条件) 和
和 合成CH3CH2CH2CH2OH的反应流程图(有机物用结构简式表示,必须注明反应条件).
合成CH3CH2CH2CH2OH的反应流程图(有机物用结构简式表示,必须注明反应条件).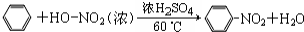 .
.