题目内容
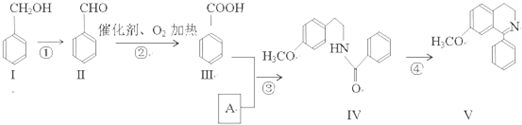
脱水环化是合成生物碱类天然产物的重要步骤,某生物碱V合成路线如下:
(1)写出IV中含氧官能团的名称 .
(2)写出IV物质的分子式
(3)写出下列反应的类型② ,③ .
(4)反应②的化学方程式 .
(5)I和III在浓硫酸催化加热时反应的化学方程式是 .
(6)下列说法正确的是 .
A.I和V均属于芳香烃
B.II能发生银镜反应
C.II能与4mol H2发生加成反应
D.反应③属于酯化反应
(7)A的结构简式 .
(8)VI与I互为同分异构体,VI遇三氯化铁溶液发生显色反应,其苯环上的一氯代物只有两种,写出满足上述条件的VI的结构简式 .

(1)写出IV中含氧官能团的名称
(2)写出IV物质的分子式
(3)写出下列反应的类型②
(4)反应②的化学方程式
(5)I和III在浓硫酸催化加热时反应的化学方程式是
(6)下列说法正确的是
A.I和V均属于芳香烃
B.II能发生银镜反应
C.II能与4mol H2发生加成反应
D.反应③属于酯化反应
(7)A的结构简式
(8)VI与I互为同分异构体,VI遇三氯化铁溶液发生显色反应,其苯环上的一氯代物只有两种,写出满足上述条件的VI的结构简式
考点:有机物的推断
专题:
分析:(1)根据Ⅳ的结构简式可知,Ⅳ中的含氧官能团为醚键和羰基;
(2)根据Ⅳ的结构简式可知其分子式;
(3)反应②是将Ⅱ中的醛基氧化成了羧基,反应③是将Ⅲ和A反应形成了肽键;
(4)反应②是苯甲醛发生氧化反应生成苯甲酸;
(5)I和III在浓硫酸催化加热时发生酯化反应生成苯甲酸苯甲酯;
(6)A.根据I和V的结构简式判断,
B.II中有醛基,能发生银镜反应,
C.II的物质的量未知,
D.反应③是形成了肽键的反应;
(7)反应③是将Ⅲ和A反应形成了肽键,比较Ⅳ和Ⅲ的结构简式可推断出A的结构;
(8)VI与I互为同分异构体,VI遇三氯化铁溶液发生显色反应,说明有酚羟基,其苯环上的一氯代物只有两种,说明有两个处于对位的基团,据此写同分异构体的结构简式.
(2)根据Ⅳ的结构简式可知其分子式;
(3)反应②是将Ⅱ中的醛基氧化成了羧基,反应③是将Ⅲ和A反应形成了肽键;
(4)反应②是苯甲醛发生氧化反应生成苯甲酸;
(5)I和III在浓硫酸催化加热时发生酯化反应生成苯甲酸苯甲酯;
(6)A.根据I和V的结构简式判断,
B.II中有醛基,能发生银镜反应,
C.II的物质的量未知,
D.反应③是形成了肽键的反应;
(7)反应③是将Ⅲ和A反应形成了肽键,比较Ⅳ和Ⅲ的结构简式可推断出A的结构;
(8)VI与I互为同分异构体,VI遇三氯化铁溶液发生显色反应,说明有酚羟基,其苯环上的一氯代物只有两种,说明有两个处于对位的基团,据此写同分异构体的结构简式.
解答:
解:(1)根据Ⅳ的结构简式可知,Ⅳ中的含氧官能团为醚键和羰基,
故答案为:醚键和羰基;
(2)根据Ⅳ的结构简式可知其分子式为C16H17NO2,
故答案为:C16H17NO2;
(3)反应②是将Ⅱ中的醛基氧化成了羧基,是氧化反应,反应③是将Ⅲ和A反应形成了肽键,是取代反应,
故答案为:氧化反应;取代反应;
(4)反应②是苯甲醛发生氧化反应生成苯甲酸,反应方程式为 ,
,
故答案为: ;
;
(5)I和III在浓硫酸催化加热时发生酯化反应生成苯甲酸苯甲酯,反应方程式为 ,
,
故答案为: ;
;
(6)A.根据I和V的结构简式可知,它们组成中除了碳氢外还都有氧元素,不属于烃类,故A错误;
B.II中有醛基,能发生银镜反应,故B正确;
C.II中有一个苯环和一个醛基都能与氢气加成,但Ⅱ的物质的量未知,故C错误;
D.反应③是形成了肽键的反应,该反应不是酯化反应,故D错误,
故选B;
(7)反应③是将Ⅲ和A反应形成了肽键,比较Ⅳ和Ⅲ的结构简式可知A的结构为 ,
,
故答案为: ;
;
(8)VI与I互为同分异构体,VI遇三氯化铁溶液发生显色反应,说明有酚羟基,其苯环上的一氯代物只有两种,说明有两个处于对位的基团,所以符合条件的Ⅰ的同分异构体的结构简式为 ,故答案为:
,故答案为: .
.
故答案为:醚键和羰基;
(2)根据Ⅳ的结构简式可知其分子式为C16H17NO2,
故答案为:C16H17NO2;
(3)反应②是将Ⅱ中的醛基氧化成了羧基,是氧化反应,反应③是将Ⅲ和A反应形成了肽键,是取代反应,
故答案为:氧化反应;取代反应;
(4)反应②是苯甲醛发生氧化反应生成苯甲酸,反应方程式为
 ,
,故答案为:
 ;
;(5)I和III在浓硫酸催化加热时发生酯化反应生成苯甲酸苯甲酯,反应方程式为
 ,
,故答案为:
 ;
;(6)A.根据I和V的结构简式可知,它们组成中除了碳氢外还都有氧元素,不属于烃类,故A错误;
B.II中有醛基,能发生银镜反应,故B正确;
C.II中有一个苯环和一个醛基都能与氢气加成,但Ⅱ的物质的量未知,故C错误;
D.反应③是形成了肽键的反应,该反应不是酯化反应,故D错误,
故选B;
(7)反应③是将Ⅲ和A反应形成了肽键,比较Ⅳ和Ⅲ的结构简式可知A的结构为
 ,
,故答案为:
 ;
;(8)VI与I互为同分异构体,VI遇三氯化铁溶液发生显色反应,说明有酚羟基,其苯环上的一氯代物只有两种,说明有两个处于对位的基团,所以符合条件的Ⅰ的同分异构体的结构简式为
 ,故答案为:
,故答案为: .
.
点评:本题考查有机物推断,流程中官能团的变化是解题的关键,需要学生熟练掌握官能团的性质,侧重考查学生分析推理与知识迁移应用能力,难度中等.

练习册系列答案
相关题目
短周期主族元素A、B、C、D、E的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,E原子最外层电子数是B原子内层电子数的3倍或者C原子最外层电子数的3倍,B、D原子最外层电子数之和等于C、E原子最外层电子数之和.下列说法正确的是( )
| A、元素A所形成的氧化物只有一种 |
| B、元素B的最高价氧化物对应的水化物为强酸 |
| C、元素C、D、E的最高价氧化物对应的水化物两两之间可发生反应 |
| D、氢化物的稳定性:A>B |
W、X、Y、Z均是短周期主族元素,X、Y、Z处于同一周期,W、X、Z的简单离子具有相同的电子层结构,W的最高价氧化物对应的水化物与其氢化物能反应生成盐,X的氧化物既能溶于酸又能溶于碱,Y的最高正价与最低负价的代数和为O.下列说法正确的是( )
| A、离子半径:W>X>Z |
| B、原子半径:Z>X>Y |
| C、单质的熔点:W>Z>Y |
| D、最高正价:Z>W>X |
-C3H7和-C3H7O取代苯环上的氢原子,形成的有机物中能与金属钠反应的同分异构体有( )
| A、10种 | B、15种 |
| C、30种 | D、36种 |
下列实验操作错误的是( )
| A、萃取、分液前需对分液漏斗检漏 |
| B、制取硝基苯时,采取水浴加热,将温度计插入水浴液中 |
| C、点燃甲烷、氢气、乙烯、CO等可燃性气体前必须验纯 |
| D、液溴保存时液面覆盖一层水,装在带橡胶塞的细口试剂瓶中 |




 ,该物质在NaOH水溶液中加热反应,可生成有机物的结构简式为
,该物质在NaOH水溶液中加热反应,可生成有机物的结构简式为 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH2=CH2
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH2=CH2