题目内容
19.某有机物2.3克,完全燃烧后的产物依次通过浓硫酸与NaOH溶液,分别增重2.7克与4.4克,该有机物可能是( )| A. | CH4 | B. | C2H4 | C. | C2H6 | D. | C2H6O |
分析 完全燃烧后的产物依次通过浓硫酸与NaOH溶液,分别增重2.7克与4.4克,可知n(H2O)=$\frac{2.7g}{18g/mol}$=0.15mol,
n(CO2)=$\frac{4.4g}{44g/mool}$=0.1mol,则有n(H)=0.3mol,m(H)=0.3g,n(C)=0.1mol,m(C)=0.1mol×12g/mol=1.2g,
结合质量守恒判断有机物中是否含有O元素,进而可计算该有机物的化学式.
解答 解:完全燃烧后的产物依次通过浓硫酸与NaOH溶液,分别增重2.7克与4.4克,可知n(H2O)=$\frac{2.7g}{18g/mol}$=0.15mol,
n(CO2)=$\frac{4.4g}{44g/mool}$=0.1mol,则有n(H)=0.3mol,m(H)=0.3g,n(C)=0.1mol,m(C)=0.1mol×12g/mol=1.2g,
则0.3g+1.2g=1.5g<2.3g,所以一定含有O元素,且m(O)=2.3g-1.5g=0.8g,n(O)=$\frac{0.8g}{16g/mol}$=0.05mol,
所以:n(C):n(H):n(O)=0.1mol:0.3mol:0.05mol=2:6:1,
故该有机物的化学式为C2H6O,
故选D.
点评 本题考查有机分子式的计算,题目难度中等,本题注意根据水和二氧化碳的质量确定有机物是否含有O元素,计算出C、H、O的原子个数比可计算出该有机物的化学式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列有关化学反应方向及其判据的说法中正确的是( )
| A. | 非自发反应就是不可能发生的反应,自发反应就是能较快进行的反应 | |
| B. | 高温高压下可以使石墨转化为金刚石是自发的化学反应 | |
| C. | 由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程 | |
| D. | 反应NH3(g)+HCl(g)═NH4Cl(s)在低温下能自发进行,说明该反应的△H>0 |
14.用下列实验装置完成对应的实验(部分仪器已省略),操作正确并能达到实验目的是( )
| A. |  制备氢氧化亚铁 | B. |  石油的分馏 | ||
| C. |  测定盐酸浓度 | D. |  配制稀硫酸 |
8.下列气体属于大气污染物的是( )
| A. | CO2 | B. | NO2 | C. | N2 | D. | H2 |
9. 近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如图所示).苯属于( )
近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如图所示).苯属于( )
 近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如图所示).苯属于( )
近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如图所示).苯属于( )| A. | 酸 | B. | 混合物 | C. | 无机物 | D. | 有机物 |
 .
.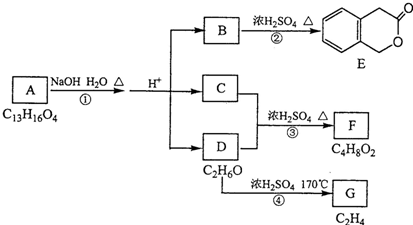
 .反应①的反应类型是水解反应或取代反应.
.反应①的反应类型是水解反应或取代反应. .
. .
. (1)指出下列能量的变化:
(1)指出下列能量的变化: