��Ŀ����
14��ijͬѧ��̽���ϸɵ���ڵĺ�ɫ�����������ʱ��������ͼ��ʾʵ�飺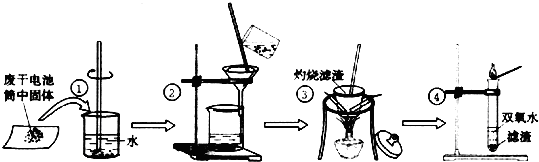
���Ľ̲Ŀ�֪����ͨп�̵�صĺ�ɫ������Ҫ�ɷ�ΪMnO2��NH4Cl��ZnCl2�����ʣ���ش��������⣺
��1�������ٵ��������ܽ⣻�����ڵ������ǹ��ˣ�
��2����������������ʱ������Ҫ�����оƾ��ơ��������������������� �����żܣ����������������еĺ�ɫ����ʱ������һ��ʹ����ʯ��ˮ����ǵ����壬�ɴ��Ʋ������л����ڵ�����ΪC��̼����
��3�������ܵ��Թܼ���������ú�ɫ�������Թ���Ѹ�ٲ�����ʹ�����ǵ�ľ����ȼ�����壬�ݴ˿ɳ����϶���ɫ����ΪMnO2��
��4����ͬѧҪ����Һ�ijɷֽ��м��飬��ȷ���Ƿ���NH4Cl��ZnCl2��������������ʵ�����д��ʵ�鱨�棬����д����հ״������ݣ�
| ʵ��Ŀ�� | ���� | ʵ������ | ���� |
| 1������Cl- | ȡ������Һ���Թ��У����������ữ����������Һ | ������ɫ���� | ����Cl- |
| 2������NH4+ | ȡ������Һ���Թ��У�����Ũ����������Һ�����ȣ�����ʪ�ĺ�ɫʯ����ֽ�����Թܿڸ��� | ʯ����ֽ����ɫ | ����NH4+��k |
| 3������Zn2+ | ȡ������Һ���Թ��У�����ϡ��ˮ | �Ȳ�����ɫ�������������백ˮ���������ܽ� | ����Zn2+ |
���� ��1���������ʼ���ˮ�������ʵ��ܽ���̣���������Һ���ù��˵ķ�����
��2�����ݶ����ʽ������չ�����Ҫ���������ƾ��ơ��������������Ǻ����żܡ��������ش�̼�������ջ����������̼��
��3����ʹ˫��ˮѸ�ٲ��������ĺ�ɫ�����Ƕ������̣�
��4�������ӵļ������������ữ����������Һ����������ɫ��������֤�����������ӣ�
笠����ӵļ�������Ũ����������Һ�����ȣ�Ȼ����ʪ��ĺ�ɫʯ����ֽ���飬������ʹʪ��ĺ�ɫʯ����ֽ����ɫ��
��� �⣺��1���������ʼ���ˮ�������ʵ��ܽ���̣���������Һ���ù��˵ķ������ʴ�Ϊ���ܽ⣻���ˣ�
��2�������ʽ������չ�����Ҫ���������ƾ��ơ��������������Ǻ����żܡ�����ʹ����ʯ��ˮ����ǵ������ж�����̼�Ͷ�����������̼���ɺ�ɫ��̼���������Ƶã�����������ɵ���ɫ�����������Ƶã����Ըú�ɫ������̼���ʣ�
�ʴ�Ϊ�������������ǣ�C��̼����
��3����ʹ�����ǵ�ľ����ȼ����������������ʹ˫��ˮѸ�ٲ��������ĺ�ɫ���������Ƕ������̣��ʴ�Ϊ��MnO2��
��4�������ӵļ��飺ȡ������Һ���Թ��У����������ữ����������Һ�������Ӻ������ӷ�Ӧ���ɲ�����ˮ�İ�ɫ�����Ȼ���������а�ɫ�������ɣ���˵���������ӣ�
笠����ӵļ��飺笠������ܺ�ǿ���ڼ��������·�Ӧ���ɰ�����������ʹʪ��ĺ�ɫʯ����ֽ����ɫ�����ʪ��ĺ�ɫʯ����ֽ����ɫ����˵����笠����Ӵ��ڣ�
�ʴ�Ϊ��
| ʵ��Ŀ�� | ���� | ʵ������ | ���� |
| 1������Cl- | ȡ������Һ���Թ��У����������ữ����������Һ | �а�ɫ�������� | ����Cl- |
| 2������NH4+ | ȡ������Һ���Թ��У�����Ũ����������Һ�����ȣ�����ʪ�ĺ�ɫʯ����ֽ�����Թܿڸ��� | ʯ����ֽ����ɫ | ����NH4+ |
���� ���⿼�����ʵķ��롢�ᴿ���ۺϲ�����Ϊ��Ƶ���㣬������ѧ���ķ���������ʵ�������Ŀ��飬��Ŀ���ؿ������ʵ����������ӵļ��飬�ѶȲ�����Ϥ��ѧ�γ����������ӵļ��鷽�����������ӡ���������ӡ������ӡ������ӡ�笠����ӵȣ�

| A�� | ���������Ʊ�����ú���� | |
| B�� | �Լ�ƿ�е�Һ�����ˮ��棬��ֹ��ӷ� | |
| C�� | ��������������Һʱ��Ҫ�����м���������������� | |
| D�� | Ũ�����ô�������ϸ�ڡ���ɫ�Լ�ƿʢ�ţ��������������� |
| A�� | Fe+2 H+=Fe3++H2�� | B�� | Fe3++Cu=Cu2++Fe2+ | ||
| C�� | Cu+2H+=Cu2++H2�� | D�� | 2Fe3++Fe=3Fe2+ |
| A�� | ${\;}_{\;}^{13}$O��14O����ͬ�������� | B�� | ������춡�黥��ͬϵ�� | ||
| C�� | ���ʯ��ʯī����ͬλ�� | D�� | 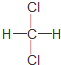 �� ��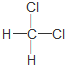 ����ͬ���칹�� ����ͬ���칹�� |
��1����������ӡˢ��·���ϵ�ͭ�Ʊ�CuCl2��
ʵ����ģ����չ������£�
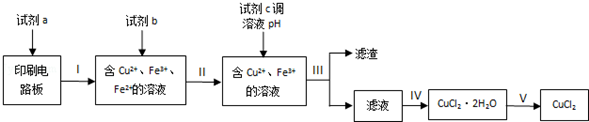
��֪�������ʿ�ʼ�����ͳ�����ȫʱ��pH���±���
| ���� | ��ʼ���� | ������ȫ |
| Fe��OH��2 | 7.6 | 9.6 |
| Fe��OH��3 | 2.7 | 3.7 |
| Cu��OH��2 | 4.4 | 8.0 |
�ٲ����IJ��������ǹ��ˣ�
�������Լ��У�������Ϊ�Լ�a����C��
A��HNO3��Һ B��Fe2��SO4��3��Һ C��FeCl3��Һ
���������Լ�b��ֱ�Ӽ����Լ�c������ҺpH���Ƿ���У�����ǡ����������Dz��ܳ�ȥFe2+��Ӱ������CuCl2���ȣ�
��2����H2O2�����Ṳͬ����ӡˢ��·���Ʊ�����ͭ��
��֪��2H2O2��l��=2H2O ��l��+O2��g����H1=-196kJ/mol
H2O��l��=H2��g��+$\frac{1}{2}$O2��g����H2=+286kJ/mol
Cu��s��+H2SO4��aq��=CuSO4��aq��+H2��g����H3=+64kJ/mol
��Cu��s��+H2O2��l��+H2SO4��aq��=CuSO4��aq��+2H2O��l����H=-320kJ/mol��
��3������ӦCu+H2O2+H2SO4=CuSO4+2H2O��Ƴ�ԭ��أ��������缫��Ӧʽ��H2O2+2H++2e-=2H2O��
��4��������������Ṳͬ����ӡˢ��·���Ʊ�����ͭ������ӡˢ��·���������ɷֲ����ᷴӦ������ȡ3mol����������ͭ����Ҫ0.5mol/L��������Һ�������4L��
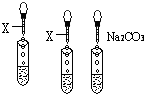 ʵ��������ƿʧȥ��ǩ����ɫ��Һ���Ȼ��ء��������ƺ�ϡ���ᣬ����һ�ֳ������ָʾ��X ��Na2CO3һ�μ������ǣ������йز����������Լ���գ�
ʵ��������ƿʧȥ��ǩ����ɫ��Һ���Ȼ��ء��������ƺ�ϡ���ᣬ����һ�ֳ������ָʾ��X ��Na2CO3һ�μ������ǣ������йز����������Լ���գ�