��Ŀ����
�ס��ҡ����������졢�����ֶ�����Ԫ��ԭ���������ε�������ԭ�������������Ǵ�������������������ԭ�ӵĴ�����������������������4�������ļ���������ͬ����Ԫ�ؼ������а뾶��С�ģ����뼺���ڣ�����ԭ�Ӱ뾶��ͬ��������Ԫ������С����ش��������⣺
��1���Ͷ��ֱ��� �� ����Ԫ�ط��ţ�
��2���Һͼ��γɵĻ������и�ԭ�ӵ�����������8�����ȶ��ṹ���仯ѧʽΪ
��3���������γ�ԭ�Ӹ�����Ϊ1��1�Ļ������У����ڵ������������� ������ȷ�𰸱�ţ�
�ټ��Լ� �ڷǼ��Լ� �����Ӽ� �����
��4����ҵȼ�ս�̿���β���к��б�������ɵ����壬Ϊ�˲ⶨ��������β���еĺ���������ѡ����Լ��ǣ�����ȷ�𰸱�ţ�
A����ˮ B������������Һ C������-�⻯����Һ D�������ữ�ĸ��������Һ
��5����ҵ��ͨ���õ�ⷨ�Ʊ����ĵ��ʣ���Ӧ�����ӷ���ʽΪ
��6�������ӹ�ҵ�У��ҵ���̬�⻯���ˮ��Һ������ʴ��H2O2�����������������Ӧ�IJ��ﲻ��Ⱦ�������仯ѧ��Ӧ����ʽΪ ��
��1���Ͷ��ֱ���
��2���Һͼ��γɵĻ������и�ԭ�ӵ�����������8�����ȶ��ṹ���仯ѧʽΪ
��3���������γ�ԭ�Ӹ�����Ϊ1��1�Ļ������У����ڵ�������������
�ټ��Լ� �ڷǼ��Լ� �����Ӽ� �����
��4����ҵȼ�ս�̿���β���к��б�������ɵ����壬Ϊ�˲ⶨ��������β���еĺ���������ѡ����Լ��ǣ�����ȷ�𰸱�ţ�
A����ˮ B������������Һ C������-�⻯����Һ D�������ữ�ĸ��������Һ
��5����ҵ��ͨ���õ�ⷨ�Ʊ����ĵ��ʣ���Ӧ�����ӷ���ʽΪ
��6�������ӹ�ҵ�У��ҵ���̬�⻯���ˮ��Һ������ʴ��H2O2�����������������Ӧ�IJ��ﲻ��Ⱦ�������仯ѧ��Ӧ����ʽΪ
���㣺λ�ýṹ���ʵ����ϵӦ��
ר�⣺Ԫ����������Ԫ�����ڱ�ר��
�������ס��ҡ����������졢�����ֶ�����Ԫ��ԭ���������ε�������ԭ�������������Ǵ�����������������ԭ��ֻ����2�����Ӳ㣬����������Ϊ4�����ΪC����ԭ�ӵĴ�����������������������4����ԭ��ֻ����2�����Ӳ㣬����������Ϊ6�����ΪO���ҵ�ԭ����������C��O֮�䣬����ΪN�����ļ���������ͬ����Ԫ�ؼ������а뾶��С�ģ�ԭ����������O��Ӧ���ڵ������ڣ�����֪��ΪAl�����뼺���ڣ�ԭ������������Al�������ڵ������ڣ�����ԭ�Ӱ뾶��ͬ��������Ԫ������С����ΪCl������ΪS���ݴ˽��
���
�⣺�ס��ҡ����������졢�����ֶ�����Ԫ��ԭ���������ε�������ԭ�������������Ǵ�����������������ԭ��ֻ����2�����Ӳ㣬����������Ϊ4�����ΪC����ԭ�ӵĴ�����������������������4����ԭ��ֻ����2�����Ӳ㣬����������Ϊ6�����ΪO���ҵ�ԭ����������C��O֮�䣬����ΪN�����ļ���������ͬ����Ԫ�ؼ������а뾶��С�ģ�ԭ����������O��Ӧ���ڵ������ڣ�����֪��ΪAl�����뼺���ڣ�ԭ������������Al�������ڵ������ڣ�����ԭ�Ӱ뾶��ͬ��������Ԫ������С����ΪCl������ΪS��
��1��������������֪���Ͷ��ֱ���C��Al���ʴ�Ϊ��C��Al��
��2��N��Cl�γɵĻ������и�ԭ�ӵ�����������8�����ȶ��ṹ��Nԭ��Ӧ�γ�3�����ۼ����仯ѧʽΪNCl3���ʴ�Ϊ��NCl3��
��3��O�����γ�ԭ�Ӹ�����Ϊ1��1�Ļ�����ΪH2O2��H2O2��Hԭ����Oԭ��֮���γɼ��Լ���Oԭ��֮���γɷǼ��Լ���H2O2����֮���γ�������ʴ�Ϊ���٢ڢܣ�
��4����ҵȼ�ս�̿���β���к��б�������ɵ�����ΪSO2������������Һ�������ն�����̼������������ȷ����������ĺ���������-�⻯����Һ�������������Ӧ��Ҳ���ⶨ������ˮ�����Ը�����ض�ֻ���������������Բⶨ��������ĺ�����
�ʴ�Ϊ��AD��
��5����ҵ��ͨ���õ�ⱥ��ʳ��ˮ�Ʊ���������Ӧ�����ӷ���ʽΪ 2Cl-+2H2O
2OH-+H2��+Cl2����
�ʴ�Ϊ��2Cl-+2H2O
2OH-+H2��+Cl2����
��6���ҵ���̬�⻯��ΪNH3�������ӹ�ҵ�У�NH3ˮ��Һ������ʴ��H2O2�����������������Ӧ�IJ��ﲻ��Ⱦ������Ӧ���ɵ�����ˮ���û�ѧ��Ӧ����ʽΪ��3H2O2+2NH3?H2O=N2��+8H2O��
�ʴ�Ϊ��3H2O2+2NH3?H2O=N2��+8H2O��
��1��������������֪���Ͷ��ֱ���C��Al���ʴ�Ϊ��C��Al��
��2��N��Cl�γɵĻ������и�ԭ�ӵ�����������8�����ȶ��ṹ��Nԭ��Ӧ�γ�3�����ۼ����仯ѧʽΪNCl3���ʴ�Ϊ��NCl3��
��3��O�����γ�ԭ�Ӹ�����Ϊ1��1�Ļ�����ΪH2O2��H2O2��Hԭ����Oԭ��֮���γɼ��Լ���Oԭ��֮���γɷǼ��Լ���H2O2����֮���γ�������ʴ�Ϊ���٢ڢܣ�
��4����ҵȼ�ս�̿���β���к��б�������ɵ�����ΪSO2������������Һ�������ն�����̼������������ȷ����������ĺ���������-�⻯����Һ�������������Ӧ��Ҳ���ⶨ������ˮ�����Ը�����ض�ֻ���������������Բⶨ��������ĺ�����
�ʴ�Ϊ��AD��
��5����ҵ��ͨ���õ�ⱥ��ʳ��ˮ�Ʊ���������Ӧ�����ӷ���ʽΪ 2Cl-+2H2O
| ||
�ʴ�Ϊ��2Cl-+2H2O
| ||
��6���ҵ���̬�⻯��ΪNH3�������ӹ�ҵ�У�NH3ˮ��Һ������ʴ��H2O2�����������������Ӧ�IJ��ﲻ��Ⱦ������Ӧ���ɵ�����ˮ���û�ѧ��Ӧ����ʽΪ��3H2O2+2NH3?H2O=N2��+8H2O��
�ʴ�Ϊ��3H2O2+2NH3?H2O=N2��+8H2O��
���������⿼��ṹ����λ�ù�ϵӦ�ã��Ѷ��еȣ��ƶ�Ԫ�غ��ƽ���ؼ������ض�ѧ���������Ŀ��飬��3��Ϊ�״��㣬ѧ�������Է����ڻ�ѧ�������Է���֮�����������

��ϰ��ϵ�д�
�����Ŀ
���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ���ǣ�������
| A��̼���Ƶ�ˮ�⣺CO32-+2H2O?H2CO3+2OH- |
| B���ƺ�ˮ��Ӧ��Na+2H2O�TNa++2OH-+H2�� |
| C���ù���������ữ�����ҽ���Һ����ȡ�⣺2I-+H2O2�TI2+2OH- |
| D����NaAlO2��Һ��ͨ�����CO2��Al��OH��3��AlO2-+CO2+2H2O�TAl��OH��3��+HCO3- |
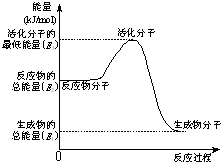 �״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ����
�״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ������CH3OH��g��+H2O��g����CO2��g��+3H2��g��-49.0kJ
��CH3OH��g��+
| 1 |
| 2 |
����˵����ȷ���ǣ�������
| A������ͼʾ�ķ�ӦΪ���ȷ�Ӧ |
| B��ͼ�е������仯��ͼ��ʾ����Q=E3-E1 |
| C��H2ȼ���ܷų��������ȣ���CH3OHת���H2�Ĺ��̱����������� |
| D�����ݢ٢���֪����25�棬101kPaʱ��1mol CH3OH��g����ȫȼ������CO2��H2O�ų�������Ӧ676.7kJ |
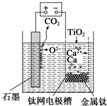 ��ͼ��ʯī������������������������CaF2-CaO������ʣ�ͼʾװ�ù���ʱ�����ɵĽ������ܻ�ԭ���������Ʊ������ѣ�����˵������ȷ���ǣ�������
��ͼ��ʯī������������������������CaF2-CaO������ʣ�ͼʾװ�ù���ʱ�����ɵĽ������ܻ�ԭ���������Ʊ������ѣ�����˵������ȷ���ǣ�������| A��������ӦʽΪC+2O2--4e-�TCO2�� |
| B����TiO2�Ƶ�1mol����Ti�����������·ת��4mol���� |
| C���Ʊ�������ǰ��װ����CaO�������� |
| D��TiO2�������ŵ� |
���н���ʵ����ʵ�ķ���ʽ��ȷ���ǣ�������
| A����ˮ�е����̪��Һ����Һ��죺NH3?H2O�TNH4++OH- |
| B��90��ʱ����ô�ˮ��c��H+��?c��OH-��=3.8��10-13��H2O��l��?H+��aq��+OH-��aq����H��0 |
| C��FeCl3��Һ��ͨ��SO2����Һ��ɫ��ȥ��2Fe3++SO2+2H2O�T2Fe2++SO42-+4H+ |
| D��������Һ��ͨ��CO2����Һ����ǣ�2C6H5ONa+CO2+H2O��2C6H5OH+Na2CO3 |
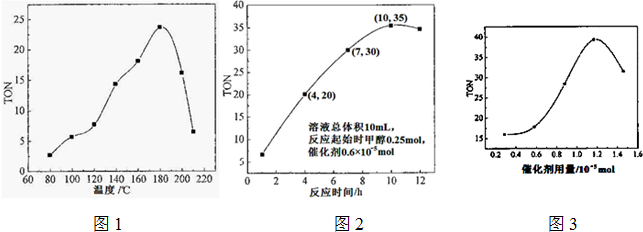
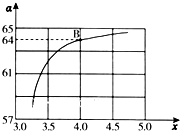 �����£�N2H4���ǵ������ֳ����⻯��ڿ�ѧ����������������Ҫ��Ӧ�ã�
�����£�N2H4���ǵ������ֳ����⻯��ڿ�ѧ����������������Ҫ��Ӧ�ã�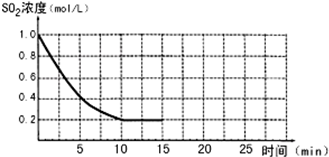 ��֪��2SO2��g��+O2��g��?2SO3��g������H=-196kJ/mol��850Kʱ����2L�̶��ݻ����ܱ������г���2mol SO2��2mol O2��10���Ӻ�ﵽƽ�⣬SO2Ũ�Ⱥ�ʱ���ϵ��ͼ��
��֪��2SO2��g��+O2��g��?2SO3��g������H=-196kJ/mol��850Kʱ����2L�̶��ݻ����ܱ������г���2mol SO2��2mol O2��10���Ӻ�ﵽƽ�⣬SO2Ũ�Ⱥ�ʱ���ϵ��ͼ�� ��һ�������£�������̼�������������·�Ӧ��
��һ�������£�������̼�������������·�Ӧ��