题目内容
6.下列变化需要加入适当的氧化剂才能实现的是( )| A. | CuO→Cu | B. | Fe→Fe2+ | C. | H2SO4→SO2 | D. | H2O2→O2 |
分析 需要加入适当的氧化剂才能实现,则选项中为还原剂的反应,还原剂中某元素的化合价升高,以此来解答.
解答 解:A.Cu元素的化合价降低,需要加还原剂实现,故A不选;
B.Fe元素的化合价升高,需要加氧化剂实现,故B选;
C.S元素的化合价降低,需要加还原剂实现,故C不选;
D.可在催化剂条件下自身发生氧化还原反应生成氧气,故D不选.
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重基本概念的考查,注意从元素化合价角度分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列叙述中,正确的是( )
| A. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| B. | 用澄清石灰水鉴别SO2 和CO2 | |
| C. | 将Fe(NO3)2 溶于稀盐酸,滴加KSCN 溶液没有颜色变化 | |
| D. | 透闪石的化学成分为Ca2Mg5Si8O22(OH)2 写成氧化物的形式为:2CaO•5MgO•8SiO2•H2O |
17.几种短周期元素的原子半径及其某些化合价见下表:
分析上表中有关数据,并结合已学过的知识,回答以下问题.涉及上述元素的答案,请用元素符号表示.
(1)E元素在周期表中位于第三周期VIA族.
(2)A、H、J对应离子的半径由大到小的顺序是(填离子符号)F->Na+>Al3+,A离子的结构示意图为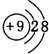 .
.
(3)上述元素的最高价氧化物对应水化物的酸性最强的为S,碱性最强的为Na(填元素符号);这两种元素形成化合物的电子式为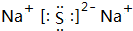 .
.
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | +4、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
(1)E元素在周期表中位于第三周期VIA族.
(2)A、H、J对应离子的半径由大到小的顺序是(填离子符号)F->Na+>Al3+,A离子的结构示意图为
 .
.(3)上述元素的最高价氧化物对应水化物的酸性最强的为S,碱性最强的为Na(填元素符号);这两种元素形成化合物的电子式为
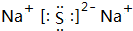 .
.
14.分子式为C5H8的有机物,不可能是( )
| A. | 只含有1个双键的直链有机物 | B. | 含有2个双键的直链有机物 | ||
| C. | 含有1个双键的环状有机物 | D. | 含有1个叁键的直链有机物 |
1.下列离子方程式正确的是( )
| A. | Na与水反应 Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向AlCl3溶液中加入过量的NaOH溶液 Al3++3OH-═Al(OH)3↓ | |
| C. | 氢氧化钡溶液与硫酸溶液反应 Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | CO2通入过量澄清石灰水 CO2+Ca2++2OH-═CaCO3↓+H2O |
15.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对大小 | |
| D. | 在一定条件下,某可逆反应正向是吸热反应,则其逆向必是放热反应 |
16.将42g纯醋酸(化学式为CH3COOH,相对分子质量为60)溶解在58g水中,形成密度为1.05g/cm3的溶液,所得溶液中醋酸的物质的量浓度为( )
| A. | 7.35 mol/L | B. | 8.70 mol/L | C. | 10.05 mol/L | D. | 11.40 mol/L |

