题目内容
20.常温下,下列各组离子一定能在指定溶液中大量共存的是( )| A. | $\frac{KW}{c(H+)}$=1×10-13 mol•L-1的溶液中:Fe2+、K+、NO3-、SO42- | |
| B. | 使酚酞试液变红色的溶液中:Na+、Ba2+、NO3-、Cl- | |
| C. | c(Fe3+)=0.1 mol•L-1的溶液中:Na+、Cl-、SCN-、SO42- | |
| D. | 水电离的c(H+)=1×10-13 mol•L-1的溶液中:K+、Na+、Br-、HCO3- |
分析 A.$\frac{KW}{c(H+)}$=1×10-13 mol•L-1的溶液,显酸性;
B.使酚酞试液变红色的溶液,显碱性;
C.离子之间结合生成络离子;
D.水电离的c(H+)=1×10-13 mol•L-1的溶液,为酸或碱溶液.
解答 解:A.$\frac{KW}{c(H+)}$=1×10-13 mol•L-1的溶液,显酸性,Fe2+、H+、NO3-发生氧化还原反应,不能共存,故A错误;
B.使酚酞试液变红色的溶液,显碱性,该组离子之间不反应,可大量共存,故B正确;
C.Fe3+、SCN-结合生成络离子,不能共存,故C错误;
D.水电离的c(H+)=1×10-13 mol•L-1的溶液,为酸或碱溶液,酸、碱溶液中均不能大量存在HCO3-,故D错误;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应、络合反应分析,题目难度不大.

练习册系列答案
相关题目
10.国际组织无机化学命名委员会将长式周期表原先的主副族族号取消,由左向右按原结构编为18列,如碱金属为第1列,稀有气体为第18列.按这个规定,下列说法不正确的是( )
| A. | 只有第2列元素的原子最外层有2个电子 | |
| B. | 第14列元素形成化合物种类最多 | |
| C. | 第3列元素种类最多 | |
| D. | 第17、18列元素都是非金属元素 |
11.短周期主族元素X、Y、Z、W的原子序数依次增大,X在元素周期表中原子半径最小,Y原子在周期表中处于族序数等于周期序数2倍的位置,Z最外层电子数是其核外电子数的3/4,W与Z属于同一主族.下列叙述正确的是( )
| A. | X与Y只能形成一种化合物 | |
| B. | 原子半径:r(Z)<r(Y)<r(W) | |
| C. | W的简单氢化物的热稳定性比Z的强 | |
| D. | Y的最高价氧化物对应的水化物是强酸 |
15.“保护环境”是我国的基本国策.下列做法不应该提倡的是( )
| A. | 化石燃料脱硫、脱硝处理 | B. | 工业废水经处理达标排放 | ||
| C. | 废电子产品统一回收处理 | D. | 农作物秸秆就地露天焚烧 |
5.下列说法正确的是( )
| A. | 实验室用Zn和稀硫酸制H2,为加快反应速率,可向稀硫酸中加入少量Cu粉 | |
| B. | CH3Cl(g)+Cl2(g)$\stackrel{光照}{→}$CH2Cl2(l)+HCl(g)常温下能自发进行,则该反应的△H>0 | |
| C. | 在一体积可变的恒温密闭容器中发生反应PCl3(g)+Cl2(g)?PCl5(g),压缩体积,平衡正向移动,K值增大 | |
| D. | 25℃时Ka(HClO)=3.0×10-8,Ka(HCN)=4.9×10-10,若该温度下NaClO溶液与NaCN溶液pH相同,则c(NaClO)<c(NaCN) |
9.某气态的烷烃与烯烃的混合气体,其密度为同状况下H2密度的11倍,1体积混合气完全燃烧生成的水蒸汽体积为2体积(在同条件下),则原混合气体的组成为( )
| A. | 甲烷,丙烯 | B. | 乙烷,乙烯 | C. | 甲烷,乙烯 | D. | 乙烷,丙烯 |
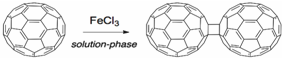

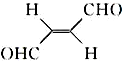 ,下列叙述正确的有AD.
,下列叙述正确的有AD.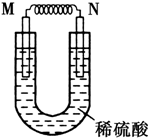 由铜片、铁片和200mL稀H2SO4组成的原电池中,若铁片只发生电化学反应,则当N极上共放出5.6L (标准状况)气体时,H2SO4恰好完全消耗.
由铜片、铁片和200mL稀H2SO4组成的原电池中,若铁片只发生电化学反应,则当N极上共放出5.6L (标准状况)气体时,H2SO4恰好完全消耗.