题目内容
13.下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )| A. | H +NO3- Fe 2+Na + | B. | Ag +NO3- Cl -K + | ||
| C. | K +Ba 2+OH -SO42- | D. | Cu 2+NH4+ Br -OH - |
分析 A.硝酸根离子在酸性条件下能够氧化亚铁离子;
B.氯离子与银离子反应生成氯化银沉淀,该反应不属于氧化还原反应;
C.钡离子与硫酸根离子反应生成硫酸钡沉淀,该反应为复分解反应;
D.铜离子与氢氧根离子反应生成氢氧化铜沉淀,该反应不属于氧化还原反应.
解答 解:A.H+、NO3-、Fe2+之间发生氧化还原反应,在溶液中不能大量共存,故A正确;
B.Ag+、Cl-之间反应生成AgCl沉淀,该反应为复分解反应,不属于氧化还原反应,故B错误;
C.Ba2+、SO42-之间反应生成难溶物硫酸钡,该反应中没有化合价变化,不属于氧化还原反应,故C错误;
D.Cu2+与OH-反应生成难溶物氢氧化铜,该反应为复分解反应,故D错误;
故选A.
点评 本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列化学用语的书写正确的是( )
| A. | 氮气的电子式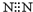 | B. | 乙烯的结构式:C2H4 | ||
| C. | 用电子式表示HCl的形成过程: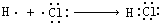 | D. | 乙醇的分子式:C2H5OH |
1.下列措施对增大反应速率明显有效的是( )
| A. | 在H202分解中加入MnO2 | |
| B. | Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸 | |
| C. | 在NaOH与HCL两溶液反应时,增大压强 | |
| D. | Na与水反应时增大水的用量 |
8.将5.4g Ag跟30.0ml 10.0mol/L的HNO3充分反应,还原产物有NO和NO2,若反应后溶液中有a molH+,则 此时溶液中含NO3-的物质的量为( )
| A. | (0.05+a) mol | B. | 0.5a mol | C. | 0.1a mol | D. | 2a mol |
5.下列叙述正确的是( )
| A. | 1 mol H2O的质量为18g/mol | B. | 3.01×1023个SO2分子的质量为32g | ||
| C. | CH4的摩尔质量为16g | D. | 44g CO2含有的O原子数为NA |
2.下列事实与元素周期律相关知识无关的是( )
| A. | 向淀粉KI 溶液中滴入溴水,溶液变蓝 | |
| B. | NaOH、Mg(OH)2、Al(OH) 3的碱性依次减弱 | |
| C. | 金属钠燃烧呈现黄色火焰,金属钾燃烧呈现紫色火焰 | |
| D. | F2和H2 暗处化合爆炸,而Cl2 和H2 化合需光照或点燃 |
3.下表是元素周期表的一部分,有关说法正确的是( )
| 族周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | a | c | e | g | |||
| 3 | b | d | f | h |
| A. | a单质的熔点、沸点比b单质高 | |
| B. | 八种元素中,b元素单质的化学性质最活泼 | |
| C. | 八种元素的单质中,常温下有五种固体 | |
| D. | c、d、f、h的最高价氧化物对应的水化物的酸性依次增强 |
