题目内容
4.硫酸亚铁是一种重要的化工产品,在工业上有重要的用途.学生探究烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备绿矾(FeSO4•7H2O式量为278),并进一步计算产品的纯度.工艺流程如下所示:
(1)烧渣在进行酸溶时用到的酸为硫酸.
(2)过程中灼烧时产生的气体通入下列溶液中,溶液不会褪色的是B
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.红色的酚酞试液
(3)X是铁粉,检验溶液Q中含有的金属阳离子的实验方法是取待测液于试管中,滴入几滴KSCN,无明显现象,滴入双氧水或氯水,溶液变血红色,则说明溶液中含有亚铁离子.
(4)操作III的操作步骤为蒸发浓缩、冷却结晶、过滤、洗涤、干燥.(填操作名称)
(5)测定绿矾产品中Fe2+含量的实验步骤:
a.称取6.0g产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01mol•L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积为40.00mL.(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O).
①标准液装在酸式滴定管中(填“酸式”或“碱式”),计算上述产品中FeSO4•7H2O的质量分数为92.7%;
②若在a步操作中,进行定容时仰视刻度线定容,则会使测得的产品中FeSO4•7H2O的质量分数偏小.(填“偏大”“偏小”或“无影响”).
分析 烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备绿矾,为了减少引入新杂质,所以用硫酸溶解并通入足量氧气,反应后过滤得到滤渣M和溶液N,滤渣M中含硫,灼烧后会产生二氧化硫,溶液N中主要溶质为硫酸铁,加入足量的铁粉反应生成硫酸亚铁,过滤除去多余的铁粉,得到硫酸亚铁溶液,将硫酸亚铁溶液蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到绿矾.
(1)本实验要制备绿矾,为了不引入新杂质,要用硫酸溶解;
(2)过程中灼烧时产生的气体为SO2,具有还原性和漂白性及酸性氧化物的通性;
(3)根据流程分析可知,溶液N中主要溶质为硫酸铁,要制得绿矾要加铁粉,检验亚铁离子可以用KSCN溶液及氧化剂,看溶液颜色的变化;
(4)从硫酸亚铁溶液中得到绿矾,要将硫酸亚铁溶液蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
(5)①高锰酸钾有强氧化性,应用酸式滴定管,根据电子得失守恒有关系式KMnO4~5FeSO4•7H2O,利用高锰酸钾的物质的量可以计算出FeSO4•7H2O的物质的量,进而确定质量分数;
②若在a步操作中,进行定容时仰视刻度线定容,则所得样品溶液浓度偏小,消耗的高锰酸钾的体积也会偏小,据此答题.
解答 解:烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备绿矾,为了减少引入新杂质,所以用硫酸溶解并通入足量氧气,反应后过滤得到滤渣M和溶液N,滤渣M中含硫,灼烧后会产生二氧化硫,溶液N中主要溶质为硫酸铁,加入足量的铁粉反应生成硫酸亚铁,过滤除去多余的铁粉,得到硫酸亚铁溶液,将硫酸亚铁溶液蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到绿矾.
(1)本实验要制备绿矾,为了不引入新杂质,要用硫酸溶解,
故答案为:硫酸;
(2)过程中灼烧时产生的气体为SO2,具有还原性和漂白性及酸性氧化物的通性,能使品红褪色,能与酸性KMnO4溶液发生氧化还原反应而使其褪色,能与碱反应使红色的酚酞试液褪色,不能使紫色石蕊溶液褪色,
故答案为:B;
(3)根据流程分析可知,溶液N中主要溶质为硫酸铁,要制得绿矾要加铁粉,反应的离子方程式为 Fe+2Fe3+=3 Fe2+,检验亚铁离子的方法是取待测液于试管中,滴入几滴KSCN,无明显现象,滴入双氧水或氯水,溶液变血红色,则说明溶液中含有亚铁离子,
故答案为:铁粉; 取待测液于试管中,滴入几滴KSCN,无明显现象,滴入双氧水或氯水,溶液变血红色,则说明溶液中含有亚铁离子;
(4)从硫酸亚铁溶液中得到绿矾,要将硫酸亚铁溶液蒸发浓缩、冷却结晶、过滤、洗涤、干燥,
故答案为:冷却结晶;洗涤;
(5)①高锰酸钾有强氧化性,应用酸式滴定管,高锰酸钾的物质的量为0.01mol•L-1×0.04L=0.0004mol,根据电子得失守恒有关系式KMnO4~5FeSO4•7H2O,则6.0g产品中含有FeSO4•7H2O的质量0.0004mol×$\frac{250}{25}$×5×278g/mol=5.56g,所以FeSO4•7H2O的质量分数为$\frac{5.56g}{6g}$×100%=92.7%,
故答案为:酸式;92.7%;
②若在a步操作中,进行定容时仰视刻度线定容,则所得样品溶液浓度偏小,消耗的高锰酸钾的体积也会偏小,根据①的计算可知测得的产品中FeSO4•7H2O的质量分数偏小,
故答案为:偏小.
点评 本题考查较为综合,涉及物质含量的测定、制备实验方案的设计等知识,题目难度中等,注意常见化学实验操作方法及实验误差分析方法.

| A. | 镁与盐酸反应放出氢气 | B. | 高锰酸钾分解 | ||
| C. | 氢氧化钠与盐酸的反应 | D. | Ba(OH)2•8H2O与NH4Cl反应 |
| A. | ①④⑤ | B. | ②③ | C. | ②③④ | D. | 只有④⑤ |
| A. | 实验室制乙烯 | B. | 苯的硝化 | C. | 银镜反应 | D. | 乙酸乙酯的制备 |
| A. | 丙烷 | B. | 丙烯 | C. | 1,3-丁二烯 | D. | 乙烷 |
| A. | H +NO3- Fe 2+Na + | B. | Ag +NO3- Cl -K + | ||
| C. | K +Ba 2+OH -SO42- | D. | Cu 2+NH4+ Br -OH - |
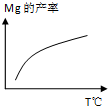 除电解法,工业炼镁还可采用硅热法(Pidgeon法).即以煅白(CaO•MgO)为原料与硅铁(含硅75%的硅铁合金)混合置于密闭还原炉,1200℃下发生反应:2(CaO•MgO)(s)+Si(s)?Ca2SiO4 (l)+2Mg(g)
除电解法,工业炼镁还可采用硅热法(Pidgeon法).即以煅白(CaO•MgO)为原料与硅铁(含硅75%的硅铁合金)混合置于密闭还原炉,1200℃下发生反应:2(CaO•MgO)(s)+Si(s)?Ca2SiO4 (l)+2Mg(g)