题目内容
某有机物A的相对分子质量是乙烷的2倍,取有机物A 6g完全燃烧后,生成8.8g CO2和3.6g 水,此化合物即可与金属钠反应,又可与氢氧化钠和碳酸钠溶液反应,计算该有机物的化学式,写出结构简式.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:有机物A的相对分子质量是乙烷的2倍,故有机物A的相对分子质量为60,根据n=
计算出CO2和H2O的物质的量,然后计算n(C)、n(H),再根据m=nM计算C原子、H原子的质量,进而确定6g有机物中是否含有O元素,并计算O原子的质量,进而计算C、H、O的物质的量比值,结合相对分子质量可得该有机物的化学式;
有机物物既可与金属钠反应,又可与氢氧化钠和碳酸钠反应,故含有-COOH或-COOH、-OH,结合有机物的分子式书写符合条件的结构.
| m |
| M |
有机物物既可与金属钠反应,又可与氢氧化钠和碳酸钠反应,故含有-COOH或-COOH、-OH,结合有机物的分子式书写符合条件的结构.
解答:
解:该有机物燃烧生成二氧化碳的物质的量为:n(CO2)=
=0.2mol,则6g有机物中:n(C)=n(CO2)=0.2mol,m(C)=0.2mol×12g/mol=2.4g,
燃烧生成水的物质的量为:n(H2O)=
=0.2mol,则6g有机物中:n(H)=2n(H2O)=0.4mol,m(H)=0.4mol×1g/mol=0.4g,
由于2.4g+0.4g=2.8g<6g,
则有机物中还应还用O元素,且氧元素的质量为:m(O)=6g-2.4g-0.4g=3.2g,物质的量为:n(O)=
=0.2mol,
则有机物中:n(C):n(H):n(O)=0.2mol:0.4mol:0.2mol=1:2:1,
所以该有机物的最简式为:CH2O;
设有机物组成为(CH2O)x,有机物A的相对分子质量是乙烷的2倍,
则有机物A的相对分子质量为60,则30x=60,解得:x=2,
所以该有机物的分子式为:C2H4O2;
有机物A分子式为C2H4O2,既可与金属钠反应,又可与氢氧化钠和碳酸钠反应,故含有-COOH,故有机物A的结构简式为:CH3COOH,
答:该有机物的分子式为C2H4O2;有机物A的结构简式为CH3COOH.
| 8.8g |
| 44g/mol |
燃烧生成水的物质的量为:n(H2O)=
| 3.6g |
| 18g/mol |
由于2.4g+0.4g=2.8g<6g,
则有机物中还应还用O元素,且氧元素的质量为:m(O)=6g-2.4g-0.4g=3.2g,物质的量为:n(O)=
| 3.2g |
| 16g/mol |
则有机物中:n(C):n(H):n(O)=0.2mol:0.4mol:0.2mol=1:2:1,
所以该有机物的最简式为:CH2O;
设有机物组成为(CH2O)x,有机物A的相对分子质量是乙烷的2倍,
则有机物A的相对分子质量为60,则30x=60,解得:x=2,
所以该有机物的分子式为:C2H4O2;
有机物A分子式为C2H4O2,既可与金属钠反应,又可与氢氧化钠和碳酸钠反应,故含有-COOH,故有机物A的结构简式为:CH3COOH,
答:该有机物的分子式为C2H4O2;有机物A的结构简式为CH3COOH.
点评:本题考查有机物分子式的确定,题目难度中等,根据生成物的质量和有机物的质量判断有机物中是否含有O元素为解答该题的关键,注意掌握常见有机物结构与性质,明确确定有机物分子式、结构简式的方法,试题有利于培养学生的分析、理解能力及化学计算能力.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
向含有7.4g Ca(OH)2的澄清石灰水中通入CO2气体后,得到8g白色沉淀,则通入的CO2气体的物质的量为( )
| A、0.08mol |
| B、0.10mol |
| C、0.12mol |
| D、0.18mol |
将铁铝矾[Al2Fe(SO4)4?xH2O]溶于水中,得到浅绿色溶液,下列有关该溶液的叙述正确的是( )
| A、铁铝矾有净水作用,其水溶液显中性 |
| B、向该溶液中加入Na2S溶液,有淡黄色沉淀 |
| C、在空气中,蒸干并灼烧该溶液,最后所得的残留固体为Al2O3、Fe2O3 |
| D、用惰性电极电解该溶液时,阴极区有沉淀 |
下列物质的用途与其化学性质相关的是( )
| A、用氮气作食品包装袋的填充气 |
| B、用金刚石切割玻璃 |
| C、用活性炭作净水剂 |
| D、用金属铝作导线 |
可把苯酚、硫氰化钾、乙醇、氢氧化钠、硝酸银等五种溶液鉴别出来的试剂是( )
| A、浓溴水 |
| B、酚酞溶液 |
| C、NaBr溶液 |
| D、FeCl3溶液 |
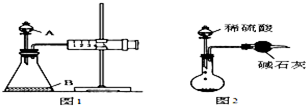 学校实验室现有含少量NaCl杂质的Na2CO3固体样品,某化学兴趣小组的同学决定测定样品Na2CO3的质量分数,甲、乙两位同学分别设计出下列两种实验方案:
学校实验室现有含少量NaCl杂质的Na2CO3固体样品,某化学兴趣小组的同学决定测定样品Na2CO3的质量分数,甲、乙两位同学分别设计出下列两种实验方案: