题目内容
将一定量的铁粉加入到一定浓度的稀硝酸中,金属恰好完全溶解,反应后溶液中存在:c(Fe2+):c(Fe3+)=3:2,则参加反应的Fe和HNO3的物质的量之比为( )
| A、1:1 | B、5:16 |
| C、2:3 | D、3:2 |
考点:离子方程式的有关计算
专题:
分析:同一溶液中,离子的浓度之比等于其物质的量之比,c(Fe2+):c(Fe3+)=3:2,所以该溶液中n(Fe2+):n(Fe3+)=3:2,根据亚铁离子和铁离子的物质的量及化学式计算作酸的硝酸的物质的量,根据氧化还原反应中得失电子数相等计算作氧化剂的硝酸的物质的量,从而计算得出铁和硝酸的物质的量之比.
解答:
解:同一溶液中,离子的浓度之比等于其物质的量之比,c(Fe2+):c(Fe3+)=3:2,所以该溶液中n(Fe2+):n(Fe3+)=3:2,设亚铁离子的物质的量为3xmol,则铁离子的物质的量为2xmol,根据化学式Fe(NO3)2、Fe(NO3)3知,起酸作用的硝酸的物质的量=3xmol×2+2xmol×3=12xmol;
氧化还原反应中得失电子数相等,即铁失去的电子数等于硝酸根离子得到的电子数,设作氧化剂的硝酸根离子的物质的量为ymol,所以3xmol×2+2xmol×3=3ymol,y=4x,所以参加反应的硝酸的物质的量=12xmol+4xmol=16xmol,根据铁元素守恒知,参加反应的铁的物质的量=3xmol+2xmol,所以参加反应的Fe和HNO3的物质的量之比为5xmol:16xmol=5:16,
故选B.
氧化还原反应中得失电子数相等,即铁失去的电子数等于硝酸根离子得到的电子数,设作氧化剂的硝酸根离子的物质的量为ymol,所以3xmol×2+2xmol×3=3ymol,y=4x,所以参加反应的硝酸的物质的量=12xmol+4xmol=16xmol,根据铁元素守恒知,参加反应的铁的物质的量=3xmol+2xmol,所以参加反应的Fe和HNO3的物质的量之比为5xmol:16xmol=5:16,
故选B.
点评:本题以氧化还原反应为载体考查了物质的量的有关计算,难度较大,明确元素守恒和得失电子守恒是解本题的关键,注意不要漏掉起酸作用的硝酸.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
某元素在化学反应中,由化合态变为游离态,则该元素( )
| A、一定被氧化 |
| B、一定被还原 |
| C、可能被氧化,也可能被还原 |
| D、化合价降低为0 |
下列图式表示正确的是( )
A、二氧化碳 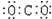 |
B、N原子的价电子电子排布图: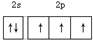 |
C、铝离子的结构示意图 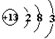 |
| D、乙醇的分子式:C2H5OH |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、标准状况下,22.4L甲烷和乙炔混合物所含的分子数约为NA |
| B、500mLl.0mol/L的乙酸溶液中含有的H+数为0.5NA |
| C、标准状况下,39 g苯中含有的碳碳双键数为1.5NA |
| D、常温常压下,22.4 L乙烯中含C-H键的数目为4NA |
下列的电离方程式,正确的是( )
| A、H2CO3═2H++CO32- |
| B、HClO?H++ClO- |
| C、Na2CO3=Na++CO32- |
| D、KOH=K++O2-+H+ |
氧气(O2)和臭氧(O3)是氧元素的两种同素异形体,已知热化学方程式:则△H1、△H2、△H3的关系正确的是( )
4Al(s)+3O2(g)═2Al2O3(s)△H1 ①
4Al(s)+2O3(g)═2Al2O3(s)△H2 ②
3O2(g)═2O3(g)△H3 ③
4Al(s)+3O2(g)═2Al2O3(s)△H1 ①
4Al(s)+2O3(g)═2Al2O3(s)△H2 ②
3O2(g)═2O3(g)△H3 ③
| A、△H1-△H2=△H3 |
| B、△H1+△H2=△H3 |
| C、△H2-△H1=△H3 |
| D、△H1+△H2+△H3=0 |
在一定温度下的定容密闭容器中,当物质的下列物理量不再发生变化时,不能表明该反应A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是( )
| A、混合气体的密度 |
| B、混合气体的总物质的量 |
| C、混合气体的平均相对分子质量 |
| D、体系的温度不变 |