题目内容
LiMO2(M为过渡金属)晶体是良好的导电材料,属六方晶系.其中Li在晶胞的顶点,三个M原子在六棱柱的三个不相邻的三角形的中线上并位于
的高度上,O原子也在这条中线上但高度分别为
和
.
(1)试画出LiMO2的一个晶胞.
(2)写出Li,M及O原子的分数坐标.
(3)这个晶胞中O原子占据的是什么空隙?占据率是多少?
| 1 |
| 2 |
| 1 |
| 4 |
| 3 |
| 4 |
(1)试画出LiMO2的一个晶胞.
(2)写出Li,M及O原子的分数坐标.
(3)这个晶胞中O原子占据的是什么空隙?占据率是多少?
考点:晶胞的计算
专题:化学键与晶体结构
分析:(1)根据完整的六方晶系图结合题中的文字说明可以画图;
(2)根据Li、M和O在三维坐系中的位置结合晶胞结构图可得分数坐标;
(3)根据O原子在晶胞的位置分析和计算;
(2)根据Li、M和O在三维坐系中的位置结合晶胞结构图可得分数坐标;
(3)根据O原子在晶胞的位置分析和计算;
解答:
解:(1)六方晶系的结构如果所示 ,当Li在晶胞的顶点,三个M原子在六棱柱的三个不相邻的三角形的中线上并位于1/2的高度上,O原子也在这条中线上但高度分别为1/4和3/4时,可得如图所示的晶胞结构图
,当Li在晶胞的顶点,三个M原子在六棱柱的三个不相邻的三角形的中线上并位于1/2的高度上,O原子也在这条中线上但高度分别为1/4和3/4时,可得如图所示的晶胞结构图 ,故答案为:
,故答案为: ;
;
(2)因为在六方晶系中二个副轴均与主轴垂直,二个副轴基向量的大小相等,副轴间的夹角为120°,Li在晶胞的顶点,所以Lii的分数坐标为(0,0,0),三个M原子在六棱柱的三个不相邻的三角形的中线上并位于1/2的高度上,所以M的分数坐标(
,
,
,),O原子在六棱柱的三个不相邻的三角形的中线上高度分别为
和
,所以O原子有两个分数坐标,分别为(
,
,
)和(
,
,
),
故答案为:Li(0,0,0),M(
,
,
),O(
,
,
)、O(
,
,
);
(3)根据晶胞的结构,在六方晶系中O原子在六棱柱的三个不相邻的三角形的中线上高度分别为1/4和3/4,将这样的氧原子占据了两个四面体空隙,其占据率为100%,故答案为:两个四面体空隙;占据分数为100%.
 ,当Li在晶胞的顶点,三个M原子在六棱柱的三个不相邻的三角形的中线上并位于1/2的高度上,O原子也在这条中线上但高度分别为1/4和3/4时,可得如图所示的晶胞结构图
,当Li在晶胞的顶点,三个M原子在六棱柱的三个不相邻的三角形的中线上并位于1/2的高度上,O原子也在这条中线上但高度分别为1/4和3/4时,可得如图所示的晶胞结构图 ,故答案为:
,故答案为: ;
;(2)因为在六方晶系中二个副轴均与主轴垂直,二个副轴基向量的大小相等,副轴间的夹角为120°,Li在晶胞的顶点,所以Lii的分数坐标为(0,0,0),三个M原子在六棱柱的三个不相邻的三角形的中线上并位于1/2的高度上,所以M的分数坐标(
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 2 |
| 1 |
| 4 |
| 3 |
| 4 |
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 4 |
| 1 |
| 3 |
| 2 |
| 3 |
| 3 |
| 4 |
故答案为:Li(0,0,0),M(
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 2 |
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 4 |
| 1 |
| 3 |
| 2 |
| 3 |
| 3 |
| 4 |
(3)根据晶胞的结构,在六方晶系中O原子在六棱柱的三个不相邻的三角形的中线上高度分别为1/4和3/4,将这样的氧原子占据了两个四面体空隙,其占据率为100%,故答案为:两个四面体空隙;占据分数为100%.
点评:本题主要考查了六方晶系的相关知识,对晶胞结构的空间想象能力要求较高,难度较大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
如图②为恒压容器,①③④为恒容容器,起始加入物如下,且起始容积均相等,维持恒温的条件下发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197KJ/mol达平衡后,各容器内放出热量Q1、Q2、Q3和Q4的大小关系正确的是( )


| A、197>Q1>Q2 |
| B、Q1>2Q3 |
| C、Q1=Q4 |
| D、Q3<Q4 |
酸雨的形成主要是由于( )
| A、森林遭到乱砍乱伐,破坏了生态环境 |
| B、汽车排出大量尾气 |
| C、大气中二氧化碳的含量增大 |
| D、含硫化石燃料的大量燃烧 |
下列有关电解质溶液中粒子的物质的量浓度关系正确的是( )
| A、在0.1mol?L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| B、在0.1mol?L-1Na2CO3溶液中:c(OH-)-c(H+)═c(HCO4-)+2c(H2CO3) |
| C、向0.2mol?L-1NaHCO3溶液中加入等体积0.1mol?L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、常温下,pH=7的CH3COONa和CH3COOH混合溶液:c(Na+)+c(CH3COO-)═c(H+)+c(OH-) |
分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些酸和醇重新组合可形成的酯共有( )
| A、28种 | B、32种 |
| C、40种 | D、48种 |
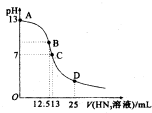 氮气是空气中含量最多的一种气体,氮气及其化合物在工农业生产、生活中有着广泛的应用.请回答下列问题:
氮气是空气中含量最多的一种气体,氮气及其化合物在工农业生产、生活中有着广泛的应用.请回答下列问题: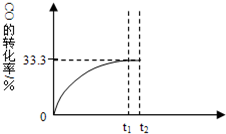 某温度下,向密闭容器中充入2.0mol CO和1.0mol H2O,发生反应:
某温度下,向密闭容器中充入2.0mol CO和1.0mol H2O,发生反应: