��Ŀ����
 �ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����壮 �ϳ����з�����ӦΪ��N2��g��+3H2��g��?2NH3��g����H��0
�ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����壮 �ϳ����з�����ӦΪ��N2��g��+3H2��g��?2NH3��g����H��0��1����ҵ����ʱ����ȡ������һ����ӦΪ��CO��g��+H2O��g��?CO2��g��+H2��g����H��0
��t��ʱ����1L�ܱ������г���0.2mol CO��0.3molˮ��������Ӧ����ƽ�����ϵ��c��H2��=0.12mol?L-1�����¶��´˷�Ӧ��ƽ�ⳣ��K=
�ڱ����¶Ȳ��䣬������ƽ����ϵ���ټ���0.1mol CO������Ӧ���½���ƽ��ʱ��ˮ��������ת���ʦ� ��H2O��=
��2���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1
| T/K | T1 | 573 | T2 |
| K | 1.00��107 | 2.45��105 | 1.88��103 |
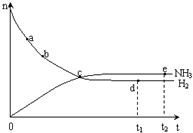
A��C���ʾn��NH3����n ��H2�����
B��C���ʾNH3����������NH3�ֽ�������ͬ
C��C���ʾ�÷�Ӧû�дﵽƽ��
D��C���ʾH2 ��NH3������Ӧ���ʴ����淴Ӧ����
��4���������з�ӦΪ��3NO2+H2O?2HNO3+NO�����������̿�������������Ҫ�����������ԭ����
���㣺���ʵ�����Ũ����ʱ��ı仯����,��ѧƽ���Ӱ������
ר�⣺��ѧƽ��ר��
��������1������������ʽ�����ƽ��ʱ�����ʵ�����ƽ��Ũ�ȣ�����ƽ�ⳣ������ʽ���㣮
�ڱ����¶Ȳ��䣬ƽ�ⳣ�����䣮������ƽ����ϵ���ټ���0.1mol CO�����Ե�ЧΪ��ʼ����0.3molCO��0.3molH2O��
��μӷ�Ӧ��ˮ�����ʵ���Ϊxmol����������ʽ��x��ʾ�������ʵ�Ũ�ȱ仯����ƽ��ʱ�����ʵ�ƽ��Ũ�ȣ�����ƽ�ⳣ������xֵ��������ת���ʶ�����㣻
��2���¶Ⱥ�ƽ�ⳣ����Ĺ�ϵȡ����ƽ�����¶ȵ�Ӱ�������
��3��A����ͼ��֪c��n��NH3����n ��H2����ȣ�
B����ͼ��֪c��������ʵ����������������ʵ�����С��c��δ����ƽ��״̬��ƽ��������Ӧ���У�
C��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶���ͬ��ƽ�ⳣ����ͬ��
D����ͼ��֪c��������ʵ����������������ʵ�����С��c��δ����ƽ��״̬��ƽ��������Ӧ���У�
��4�����������NOת��ΪNO2������NO��Ũ�ȣ�����NO2��Ũ�ȣ�ƽ��������Ӧ�ƶ������������ԭ�������ʣ�
�ڱ����¶Ȳ��䣬ƽ�ⳣ�����䣮������ƽ����ϵ���ټ���0.1mol CO�����Ե�ЧΪ��ʼ����0.3molCO��0.3molH2O��
��μӷ�Ӧ��ˮ�����ʵ���Ϊxmol����������ʽ��x��ʾ�������ʵ�Ũ�ȱ仯����ƽ��ʱ�����ʵ�ƽ��Ũ�ȣ�����ƽ�ⳣ������xֵ��������ת���ʶ�����㣻
��2���¶Ⱥ�ƽ�ⳣ����Ĺ�ϵȡ����ƽ�����¶ȵ�Ӱ�������
��3��A����ͼ��֪c��n��NH3����n ��H2����ȣ�
B����ͼ��֪c��������ʵ����������������ʵ�����С��c��δ����ƽ��״̬��ƽ��������Ӧ���У�
C��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶���ͬ��ƽ�ⳣ����ͬ��
D����ͼ��֪c��������ʵ����������������ʵ�����С��c��δ����ƽ��״̬��ƽ��������Ӧ���У�
��4�����������NOת��ΪNO2������NO��Ũ�ȣ�����NO2��Ũ�ȣ�ƽ��������Ӧ�ƶ������������ԭ�������ʣ�
���
�⣺��1����C0+H2O��g��?CO2+H2��
��ʼŨ�ȣ�0.2 0.3 0 0
�仯Ũ�ȣ�0.12 0.12 0.12 0.12
ƽ��Ũ�ȣ�0.08 0.28 0.12 0.12
��ѧƽ�ⳣ��K=
=
=1��
�ʴ�Ϊ��1��
�ڱ����¶Ȳ��䣬������ƽ����ϵ���ټ���0.1molCO���൱�ڳ���0.3molCO��0.3molˮ��������H2O��ת����xmol
CO+H2O��g��?CO2 +H2
��ʼ��0.3 0.3 0 0
ת����x x x x
ƽ��0.3-x 0.3-x x x
��
=1��
x=0.15��
ˮ��������ת���ʦ� ��H2O��=
=50%��
�ʴ�Ϊ��50%��
��2�����ڷ��ȷ�Ӧ���¶�Խ�ߣ���ѧƽ�������ƶ�������ƽ�ⳣ����С������T1��573K���ʴ�Ϊ������
��3��A����ͼ��֪c��n��NH3����n ��H2����ȣ���A��ȷ��
B����ͼ��֪c��������ʵ����������������ʵ�����С��c��δ����ƽ��״̬��ƽ��������Ӧ���У�c���ʾNH3�������ʴ���NH3�ֽ����ʣ���B����
C���¶���ͬ��ƽ�ⳣ����ͬ��e���d��ʱ��Ӧ��ƽ�ⳣ����ͬ����C��ȷ��
D����ͼ��֪c��������ʵ����������������ʵ�����С��c��δ����ƽ��״̬��ƽ��������Ӧ���У�c��ʱ����Ӧ���ʴ����淴Ӧ���ʣ���D��ȷ��
��ѡ��ACD��
��4�����������������Ũ������NOת��ΪNO2����ƽ��������Ӧ�����ƶ������������ԭ�������ʣ�
�ʴ�Ϊ�����������NOת��ΪNO2�����������ԭ�������ʣ�
��ʼŨ�ȣ�0.2 0.3 0 0
�仯Ũ�ȣ�0.12 0.12 0.12 0.12
ƽ��Ũ�ȣ�0.08 0.28 0.12 0.12
��ѧƽ�ⳣ��K=
| c(H2)?c(CO2) |
| c(CO)?c(H2O) |
| 0.12��0.12 |
| 0.08��0.08 |
�ʴ�Ϊ��1��
�ڱ����¶Ȳ��䣬������ƽ����ϵ���ټ���0.1molCO���൱�ڳ���0.3molCO��0.3molˮ��������H2O��ת����xmol
CO+H2O��g��?CO2 +H2
��ʼ��0.3 0.3 0 0
ת����x x x x
ƽ��0.3-x 0.3-x x x
��
| x2 |
| (0.3-x)2 |
x=0.15��
ˮ��������ת���ʦ� ��H2O��=
| 0.15 |
| 0.3 |
�ʴ�Ϊ��50%��
��2�����ڷ��ȷ�Ӧ���¶�Խ�ߣ���ѧƽ�������ƶ�������ƽ�ⳣ����С������T1��573K���ʴ�Ϊ������
��3��A����ͼ��֪c��n��NH3����n ��H2����ȣ���A��ȷ��
B����ͼ��֪c��������ʵ����������������ʵ�����С��c��δ����ƽ��״̬��ƽ��������Ӧ���У�c���ʾNH3�������ʴ���NH3�ֽ����ʣ���B����
C���¶���ͬ��ƽ�ⳣ����ͬ��e���d��ʱ��Ӧ��ƽ�ⳣ����ͬ����C��ȷ��
D����ͼ��֪c��������ʵ����������������ʵ�����С��c��δ����ƽ��״̬��ƽ��������Ӧ���У�c��ʱ����Ӧ���ʴ����淴Ӧ���ʣ���D��ȷ��
��ѡ��ACD��
��4�����������������Ũ������NOת��ΪNO2����ƽ��������Ӧ�����ƶ������������ԭ�������ʣ�
�ʴ�Ϊ�����������NOת��ΪNO2�����������ԭ�������ʣ�
������������һ����ҵ�ϳɰ����ۺ���֪ʶ��Ŀ����Ŀ�ѶȽϴ�ע����������ʽ������ر��Ǹ�˹���ɵ����ã�

��ϰ��ϵ�д�
�����Ŀ
�������Ӽ���ķ�����ȷ���ǣ�������
| A��ij����Һ����AgNO3��Һ�����ɰ�ɫ������˵��ԭ��Һ����Cl- |
| B��ij����Һ����BaCl2��Һ�����ɰ�ɫ������˵��ԭ��Һ����SO42- |
| C��ij����Һ����CaCl2��Һ�����ɰ�ɫ������˵��ԭ��Һ����CO32- |
| D��ij����Һ����NaOH��Һ��������ɫ������˵��ԭ��Һ����Cu2+ |
����ˮ���������ж��֣�����ɱ������ǿ���ֲ�Ӱ��ˮ�ʵ������������ǣ�������
| A������ | B��Ư�� |
| C������ | D���������� |
 ��֪CO2����������ɫȼ�ϼ״���CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-187.4kJ/mol��3000Cʱ�ĺ����ܱ������У���C��CO2��=1.00mol��L-1C��H2��=1.60mol��L-1��ʼ��Ӧ�������ͼ��ʾ���ش��������⣺
��֪CO2����������ɫȼ�ϼ״���CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-187.4kJ/mol��3000Cʱ�ĺ����ܱ������У���C��CO2��=1.00mol��L-1C��H2��=1.60mol��L-1��ʼ��Ӧ�������ͼ��ʾ���ش��������⣺ ��ͼ��1mol NO2��g����1mol CO��g����Ӧ����CO2��NO�����е������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯��
��ͼ��1mol NO2��g����1mol CO��g����Ӧ����CO2��NO�����е������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯��