题目内容
与c(H+)?c(OH-)=KW类似,FeS饱和溶液中有:c(Fe2+)?c(S2-)=KSP,已知:FeS的KSP=6.25×10-18.
(1)饱和FeS溶液的物质的量浓度为
(2)已知H2S饱和溶液中,c(H+)与c(S2-)间存在以下限量关系:{c(H+)}2?c(s2-)=1.0×10-22,现将适量FeS投入其饱和溶液中,要使溶液里c(Fe2+)=1.0mol/L,应调节溶液的pH为 .(lg2=0.3010 lg3=0.4771)
(1)饱和FeS溶液的物质的量浓度为
(2)已知H2S饱和溶液中,c(H+)与c(S2-)间存在以下限量关系:{c(H+)}2?c(s2-)=1.0×10-22,现将适量FeS投入其饱和溶液中,要使溶液里c(Fe2+)=1.0mol/L,应调节溶液的pH为
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:(1)根据FeS的KSP计算饱和FeS溶液的物质的量浓度;
(2)根据硫化亚铁的溶度积常数和亚铁离子浓度计算硫离子浓度,再根据氢硫酸的电离平衡常数计算氢离子浓度,最后利用pH计算公式计算溶液的pH.
(2)根据硫化亚铁的溶度积常数和亚铁离子浓度计算硫离子浓度,再根据氢硫酸的电离平衡常数计算氢离子浓度,最后利用pH计算公式计算溶液的pH.
解答:
解:(1)c(Fe2+)?c(S2-)=KSP,c2(FeS)=6.25×10-18,c(FeS)=2.5×10-9mol?L-1,故答案为:2.5×10-9mol?L-1;
(2)若c(Fe2+)=1.0mol?L-1则c(S2-)=
=6.25×10-18mol?L-1,c(H+)=
=4×10-3mol?L-1,pH=-lg4×10-3=2.4,
故答案为:2.4.
(2)若c(Fe2+)=1.0mol?L-1则c(S2-)=
| 6.25×10-18 |
| 1.0 |
|
故答案为:2.4.
点评:本题考查了pPH计算,根据溶度积常数及弱酸的电离平衡常数进行溶液的pH计算是解答的关键,题目难度不大.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案
相关题目
将等物质的量的A、B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g)?xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.25mol?L-1?min-1,下列说法正确的是( )
| A、反应速率v(B)=0.25 mol?L-1?min-1 |
| B、该反应方程式中,x=1 |
| C、2min时,A的物质的量为1.5mol |
| D、2min时,A的转化率为60% |
某新型手机采用甲醇-氧气燃料电池,以强碱溶液作为电解质,可连续使用一个月.该电池反应为:2CH3OH+3O2+4OH-
2CO
+6H2O,则有关说法正确的是( )
| ||
| 充电 |
2- 3 |
| A、充电时阴极发生氧化反应 |
| B、放电时负极的电极反应式为CH3OH+8OH--6e-═CO32-+6H2O |
| C、通入0.25 mol氧气并完全反应后,有0.5 mol e-转移 |
| D、放电一段时间后,通入氧气的电极附近溶液的pH升高 |
下列过程或现象与水解无关的是( )
| A、纯碱溶液去油污 |
| B、配制氯化铁溶液时加入少量的盐酸 |
| C、NaHCO3与Al2(SO4)3混合作泡沫灭火剂 |
| D、铁在潮湿的环境下生锈 |
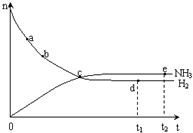 合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:N2(g)+3H2(g)?2NH3(g)△H<0
合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:N2(g)+3H2(g)?2NH3(g)△H<0