题目内容
下列叙述不正确的是( )
| A、Na、Mg、Al的第一电离能依次减弱 |
| B、H2S、H2O、HF的稳定性依次增强 |
| C、NaOH、Mg(OH)2、Al(OH)3的碱性依次减弱 |
| D、H4SiO4、H2CO3、H2SO4酸性依次增强 |
考点:金属在元素周期表中的位置及其性质递变的规律,非金属在元素周期表中的位置及其性质递变的规律,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.金属越活泼,第一电离能越大,但Mg的2s为全满,较稳定;
B.非金属性越强,气态氢化物越稳定;
C.金属性越强,最高价氧化物的水化物碱性越强;
D.非金属性越强,最高价氧化物的水化物酸性越强.
B.非金属性越强,气态氢化物越稳定;
C.金属性越强,最高价氧化物的水化物碱性越强;
D.非金属性越强,最高价氧化物的水化物酸性越强.
解答:
解:A.金属越活泼,第一电离能越大,但Mg的2s为全满,较稳定,则Na、Mg、Al的第一电离能为Mg>Al>Na,故A错误;
B.非金属性F>O>S,则H2S、H2O、HF的稳定性依次增强,故B正确;
C.金属性Na>Mg>Al,NaOH、Mg(OH)2、Al(OH)3的碱性依次减弱,故C正确;
D.非金属性S>C>Si,H4SiO4、H2CO3、H2SO4酸性依次增强,故D正确;
故选A.
B.非金属性F>O>S,则H2S、H2O、HF的稳定性依次增强,故B正确;
C.金属性Na>Mg>Al,NaOH、Mg(OH)2、Al(OH)3的碱性依次减弱,故C正确;
D.非金属性S>C>Si,H4SiO4、H2CO3、H2SO4酸性依次增强,故D正确;
故选A.
点评:本题考查金属性、非金属性的比较,为高频考点,把握元素周期律及非金属性、金属性的比较方法为解答的关键,侧重规律性知识的应用,注意A中Mg的2s电子全满为稳定结构为解答的易错点,题目难度不大.

练习册系列答案
相关题目
 mA(s)+nB(g)?qC(g),的可逆反应,在1×105pa与2×105pa两种压力条件下,B的体积分数与温度的关系如右图所示,有关叙述正确的是( )
mA(s)+nB(g)?qC(g),的可逆反应,在1×105pa与2×105pa两种压力条件下,B的体积分数与温度的关系如右图所示,有关叙述正确的是( )| A、△H>0 |
| B、X点,v正>v逆;Y点,v正<v逆 |
| C、m+n>q? |
| D、X点比Y点反应速率快 |
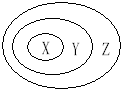 下列各选项中,各类物质依次表示为X、Y、Z,其中与如图三个圆所示的从属关系不相符的是( )
下列各选项中,各类物质依次表示为X、Y、Z,其中与如图三个圆所示的从属关系不相符的是( )| A、置换反应、氧化还原反应、化学反应 |
| B、胶体、溶液、混合物 |
| C、NaOH、电解质、化合物 |
| D、Fe2O3、金属氧化物、氧化物 |
下列现象或事实可用同一原理解释的是( )
| A、浓硫酸和浓盐酸长期暴露在空气中浓度降低 |
| B、氯水和活性炭使红墨水褪色 |
| C、漂白粉和水玻璃长期暴露在空气中变质 |
| D、次氯酸钠溶液和氯化铵溶液中水的电离均受到促进 |
关于元素周期元素,下列说法正确的是( )
| A、元素周期表有7横行被称为7个周期 |
| B、元素周期表有18纵行被称为18个族 |
| C、第IA族全部为金属元素 |
| D、每周期元素种类数目相同 |
关于淀粉和纤维素的叙述中正确的是( )
| A、化学式相同,互为同分异构体 |
| B、具有相同的最简式,互为同系物 |
| C、具有相同的化学性质 |
| D、水解反应的最终产物相同 |
下列物质分子中的氢原子不在同一平面上的有( )
| A、C2H2 |
| B、C2H4 |
| C、C2H6 |
| D、C6H6 |
下列物质中,能够导电,但不属于电解质的是( )
| A、NaOH固体 | B、稀盐酸 |
| C、熔化的NaCl | D、蔗糖 |