题目内容
高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂.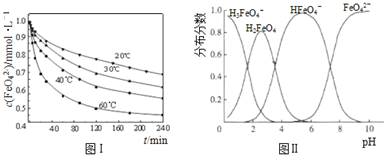
(1)已知:4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2.K2FeO4在处理水的过程中所起的作用有 .
(2)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-)=1.0mmol?L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅰ.该实验的目的是 ;发生反应的△H 0(填“>”、“<”或“=”).
(3)FeO42-在水溶液中的存在形态如图Ⅱ所示.下列说法正确的是 (填字母).
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数逐渐增大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:
HFeO4-+OH-=FeO42-+H2O
(4)测定某K2FeO4溶液浓度的实验步骤如下:
步骤1:准确量取V mL K2FeO4溶液加入到锥形瓶中
步骤2:在强碱性溶液中,用过量CrO2-与FeO42-反应生成Fe(OH)3和CrO42-
步骤3:加稀硫酸,使CrO42-转化为Cr2O72-,CrO2-转化为Cr3+,Fe(OH)3转化为Fe3+
步骤4:加入二苯胺磺酸钠作指示剂,用c mol?L-1 (NH4)2Fe(SO4)2标准溶液滴定至终点,消耗
(NH4)2Fe(SO4)2溶液V1 mL.滴定时发生的反应为:Fe2++Cr2O72-+H+→Fe3++Cr3++H2O(未配平)
①写出步骤2中发生反应的离子方程式 .
②根据上述实验数据,测定该溶液中K2FeO4的浓度为 mol?L-1(用含字母的代数式表示).

(1)已知:4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2.K2FeO4在处理水的过程中所起的作用有
(2)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-)=1.0mmol?L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅰ.该实验的目的是
(3)FeO42-在水溶液中的存在形态如图Ⅱ所示.下列说法正确的是
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数逐渐增大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:
HFeO4-+OH-=FeO42-+H2O
(4)测定某K2FeO4溶液浓度的实验步骤如下:
步骤1:准确量取V mL K2FeO4溶液加入到锥形瓶中
步骤2:在强碱性溶液中,用过量CrO2-与FeO42-反应生成Fe(OH)3和CrO42-
步骤3:加稀硫酸,使CrO42-转化为Cr2O72-,CrO2-转化为Cr3+,Fe(OH)3转化为Fe3+
步骤4:加入二苯胺磺酸钠作指示剂,用c mol?L-1 (NH4)2Fe(SO4)2标准溶液滴定至终点,消耗
(NH4)2Fe(SO4)2溶液V1 mL.滴定时发生的反应为:Fe2++Cr2O72-+H+→Fe3++Cr3++H2O(未配平)
①写出步骤2中发生反应的离子方程式
②根据上述实验数据,测定该溶液中K2FeO4的浓度为
考点:物质的量或浓度随时间的变化曲线,氧化还原反应,探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂,起到杀菌消毒作用,形成胶体具有吸附悬浮杂质的作用;
(2)温度越高,相同时间内FeO42-浓度变化越快,高铁酸钾溶液平衡时FeO42-浓度越小;温度越高FeO42-浓度越小,正向反应是吸热反应;
(3)根据图象的内容来分析图象所描述的意义;
(4)①滴定时,Cr2O72-具有很强的氧化性,能将亚铁离子氧化为三价铁离子,写出离子方程式;②根据K2FeO4溶液和(NH4)2Fe(SO4)2标准溶液量的关系,可得出原溶液中K2FeO4的浓度.
(2)温度越高,相同时间内FeO42-浓度变化越快,高铁酸钾溶液平衡时FeO42-浓度越小;温度越高FeO42-浓度越小,正向反应是吸热反应;
(3)根据图象的内容来分析图象所描述的意义;
(4)①滴定时,Cr2O72-具有很强的氧化性,能将亚铁离子氧化为三价铁离子,写出离子方程式;②根据K2FeO4溶液和(NH4)2Fe(SO4)2标准溶液量的关系,可得出原溶液中K2FeO4的浓度.
解答:
解:(1)高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂,起到杀菌消毒作用,形成胶体具有吸附悬浮杂质的作用,
故答案为:杀菌消毒、吸附悬浮物;
(2)由图1数据可知,温度越高,相同时间内FeO42-浓度变化越快,高铁酸钾溶液平衡时FeO42-浓度越小,温度越高FeO42-浓度越小,正向反应是吸热反应,
故答案为:探究温度对FeO42-浓度的影响;>;
(3)A、不同PH值时,溶液中铁元素的存在形态及种数不相同,比如在PH值等于6时,就只有两种形态,故A错误;
B、向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数先增大随后又减小,故B错误;
C、pH=6的这种溶液中,铁元素的存在形态有HFeO4-和FeO42-,加KOH溶液,只有HFeO4-能反应,发生反应的离子方程式为:HFeO4-+OH-=FeO42-+H2O,故C正确;
故答案为:C;
(4)①滴定时,Cr2O72-具有很强的氧化性,能将亚铁离子氧化为三价铁离子,发生反应的离子方程式为:6Fe2++Cr2O2-7+14H+=6Fe3++2Cr3++7H2O,
故答案为:6Fe2++Cr2O2-7+14H+=6Fe3++2Cr3++7H2O;
②在强碱性溶液中,用过量CrO-2与FeO2-4反应生成Fe(OH)3和CrO42-,CrO2-+FeO42-+2H2O=Fe(OH)3↓+CrO42-+OH-,滴定时,发生反应的离子方程式为:6Fe2++Cr2O2-7+14H+=6Fe3++2Cr3++7H2O,根据K2FeO4溶液和(NH4)2Fe(SO4)2标准溶液量的关系,可得出原溶液中K2FeO4的浓度为
mol/l,故答案为:
.
故答案为:杀菌消毒、吸附悬浮物;
(2)由图1数据可知,温度越高,相同时间内FeO42-浓度变化越快,高铁酸钾溶液平衡时FeO42-浓度越小,温度越高FeO42-浓度越小,正向反应是吸热反应,
故答案为:探究温度对FeO42-浓度的影响;>;
(3)A、不同PH值时,溶液中铁元素的存在形态及种数不相同,比如在PH值等于6时,就只有两种形态,故A错误;
B、向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数先增大随后又减小,故B错误;
C、pH=6的这种溶液中,铁元素的存在形态有HFeO4-和FeO42-,加KOH溶液,只有HFeO4-能反应,发生反应的离子方程式为:HFeO4-+OH-=FeO42-+H2O,故C正确;
故答案为:C;
(4)①滴定时,Cr2O72-具有很强的氧化性,能将亚铁离子氧化为三价铁离子,发生反应的离子方程式为:6Fe2++Cr2O2-7+14H+=6Fe3++2Cr3++7H2O,
故答案为:6Fe2++Cr2O2-7+14H+=6Fe3++2Cr3++7H2O;
②在强碱性溶液中,用过量CrO-2与FeO2-4反应生成Fe(OH)3和CrO42-,CrO2-+FeO42-+2H2O=Fe(OH)3↓+CrO42-+OH-,滴定时,发生反应的离子方程式为:6Fe2++Cr2O2-7+14H+=6Fe3++2Cr3++7H2O,根据K2FeO4溶液和(NH4)2Fe(SO4)2标准溶液量的关系,可得出原溶液中K2FeO4的浓度为
| cV1 |
| 3V |
| cV1 |
| V |
点评:本题考查学生阅读题目获取信息的能力、氧化还原反应和化学平衡移动等,难度中等,要求学生要有扎实的基础知识和灵活运用知识解决问题的能力,注意基础知识的全面掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在一定温度下,反应A2(g)+B2(g)?2AB(g)达到平衡的标志是( )
| A、单位时间内生成nmol A2,同时生成nmol AB |
| B、容器内总压强不随时间改变 |
| C、单位时间内生成2nmol AB同时生成nmol B2 |
| D、任何时间内A2、B2的物质的量之比为定值 |