题目内容
现有下列十种物质:①O2 ②Fe ③CaO ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧硫酸钠溶液 ⑨稀硝酸 ⑩Cu2(OH)2CO3.
(1)按物质的树状分类法填写表格的空白处:
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学反应方程式为 .
(3)③与⑨发生反应的离子方程式为 .
(4)②与⑨发生化学反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,该反应的还原产物是 (填化学式),氧化剂与还原剂的物质的量之比为 .
(1)按物质的树状分类法填写表格的空白处:
| 分类标准 | 氧化物 | 电解质 | |||
| 属于该类的物质 | ② | ⑧⑨ | ⑦ |
(3)③与⑨发生反应的离子方程式为
(4)②与⑨发生化学反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,该反应的还原产物是
考点:酸、碱、盐、氧化物的概念及其相互联系,离子方程式的书写,氧化还原反应的计算,电解质与非电解质
专题:物质的分类专题,氧化还原反应专题
分析:(1)根据物质的分类标准以及分类结果进行判断物质所属的类别;
(2)发生离子反应:H++OH-=H2O,是强酸强碱发生反应生成溶于水的盐;
(3)氧化钙和稀硝酸反应生成硝酸钙和水;
(4)依据化学方程式中元素化合价变化分析,元素化合价降低的物质做氧化剂,元素化合价升高的物质做还原剂,依据电子守恒计算氧化剂和还原剂物质的量之比.
(2)发生离子反应:H++OH-=H2O,是强酸强碱发生反应生成溶于水的盐;
(3)氧化钙和稀硝酸反应生成硝酸钙和水;
(4)依据化学方程式中元素化合价变化分析,元素化合价降低的物质做氧化剂,元素化合价升高的物质做还原剂,依据电子守恒计算氧化剂和还原剂物质的量之比.
解答:
解:(1)根据物质的元素组成,可以将物质分为纯净物和混合物,纯净物中,根据组成元素的种类可以将物质分为单质和化合物,只有一种元素组成的纯净物是单质,如氧气、铁,根据化合物的性质,可以将化合物分为酸、碱、盐、氧化物,如氧化钙、二氧化碳属于氧化物,根据混合物分散质微粒直径的大小,可以将混合物分为溶液(如硫酸钠溶液、稀硝酸)浊液和胶体(如红褐色的氢氧化铁液体)三种,化合物在水溶液或是熔融态下是否导电,可以将化合物分为电解质和非电解质,如CaO、H2SO4、Ba(OH)2、Cu2(OH)2CO3属于电解质,故答案为:
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,说明是强酸强碱反应生成溶于水的盐的离子反应,氢氧化钡和稀硝酸反应符合,该离子反应对应的化学方程式为Ba(OH)2+2HNO3=Ba(NO3)2+2H2O,
故答案为:Ba(OH)2+2HNO3=Ba(NO3)2+2H2O;
(3)③CaO与⑨稀硝酸发生反应生成硝酸钙和水,氧化物不能拆成离子,反应的离子方程式为CaO+2H+=Ca2++H2O,
故答案为:CaO+2H+=Ca2++H2O;
(4)②与⑨发生化学反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,反应中铁元素化合价从0价变化为+2价,化合价升高失电子做还原剂被氧化,得到氧化产物Fe(NO3)2,硝酸中氮元素化合价从+5价变化为+2价,元素化合价降低做氧化剂被还原得到还原产物NO,该反应的还原产物是NO,3molFe失电子6mol,2molHNO3得到6mol电子,氧化剂与还原剂的物质的量之比为2:3,
故答案为:NO; 2:3.
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 | ③④ | ③⑤⑥⑩ |
故答案为:Ba(OH)2+2HNO3=Ba(NO3)2+2H2O;
(3)③CaO与⑨稀硝酸发生反应生成硝酸钙和水,氧化物不能拆成离子,反应的离子方程式为CaO+2H+=Ca2++H2O,
故答案为:CaO+2H+=Ca2++H2O;
(4)②与⑨发生化学反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,反应中铁元素化合价从0价变化为+2价,化合价升高失电子做还原剂被氧化,得到氧化产物Fe(NO3)2,硝酸中氮元素化合价从+5价变化为+2价,元素化合价降低做氧化剂被还原得到还原产物NO,该反应的还原产物是NO,3molFe失电子6mol,2molHNO3得到6mol电子,氧化剂与还原剂的物质的量之比为2:3,
故答案为:NO; 2:3.
点评:本题考查了物质分类的依据和分析判断,化学方程式、离子方程式书写方法,物质组成和性质是解题关键,题目难度中等.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案
相关题目
下列的晶体中,化学键种类相同,晶体类型也相同的是( )
| A、SO2与SiO2 |
| B、CCl4与SiC |
| C、CO2与H2O |
| D、金刚石与HCl |
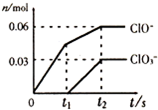 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A、苛性钾溶液中KOH的质量是16.8g |
| B、氯气在反应中既是氧化剂也是还原剂 |
| C、最终消耗氯气的物质的量为0.09mol |
| D、ClO3-的生成是由于温度升高引起的 |