题目内容
在一定温度下,反应A2(g)+B2(g)?2AB(g)达到平衡的标志是( )
| A、单位时间内生成nmol A2,同时生成nmol AB |
| B、容器内总压强不随时间改变 |
| C、单位时间内生成2nmol AB同时生成nmol B2 |
| D、任何时间内A2、B2的物质的量之比为定值 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、单位时间内生成nmol A2,等效于单位时间内消耗2nmol AB同时生成nmol AB,正逆反应速率不相等,故A错误;
B、从反应开始到平衡容器内总压强始终不变,故B错误;
C、单位时间内生成2nmol AB,等效于单位时间内消耗nmol B2同时生成nmol B2,正逆反应速率相等,故C正确;
D、任何时间内A2、B2的物质的量之比为定值,而不是不变,故D错误;
故选C.
B、从反应开始到平衡容器内总压强始终不变,故B错误;
C、单位时间内生成2nmol AB,等效于单位时间内消耗nmol B2同时生成nmol B2,正逆反应速率相等,故C正确;
D、任何时间内A2、B2的物质的量之比为定值,而不是不变,故D错误;
故选C.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
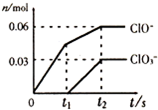 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A、苛性钾溶液中KOH的质量是16.8g |
| B、氯气在反应中既是氧化剂也是还原剂 |
| C、最终消耗氯气的物质的量为0.09mol |
| D、ClO3-的生成是由于温度升高引起的 |
下列物质中,含有共价键的离子化合物是( )
| A、NaOH |
| B、H2 |
| C、CaCl2 |
| D、Na2S |
常温常压下,用等质量的CH4、CO2、O2、SO2分别吹出如图四个气球,其中气体为CH4的是( ) 

| A、图中A为CH4、B为CO2 |
| B、图中A为SO2、C为O2 |
| C、图中B为CO2、D为CH4 |
| D、图中C为CH4、D为O2 |
R元素的原子,其最外层电子数是次外层的电子数的2倍,则R是( )
| A、S | B、Si | C、Na | D、C |
常温下pH=3的盐酸与pH=9的NaOH溶液等体积混合(假设体积等于混合前两溶液体积和),混合溶液中c(H+)的计算式是( )
A、
| ||
B、
| ||
C、
| ||
| D、以上计算式都不对 |