题目内容
6.图为元素周期表的一部分,请根据元素①-⑧在表中的位置,用化学用语回答下列问题:| 族 周期 | IA | 0 | ||||||
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)④、⑤、⑥的简单离子半径由大到小的顺序是O2->Na+>Al3+ (用离子符号表示).
(3)由①、④、⑤、三种元素组成的化合物中化学键的类型有:离子键、共价键.
(4)请写出涉及上述有关元素的两个置换反应(要求:同一反应中两种单质对应元素既不同周期也不同主族)2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO或Mg+H2SO4=MgSO4+H2↑;
(5)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:
A$→_{反应①}^{+X一定条件}$B$→_{反应②}^{+X一定条件}$C
若A、B、C含同一金属元素,X为强电解质,且反应都在溶液中进行.B的化学式为Al(OH)3.
对应的反应①的离子方程式为Al3++3OH-=Al(OH)3↓或【Al(OH)4】-+H+=Al(OH)3↓+H2O.
分析 由元素在周期表中的位置可知,①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是S,
(1)上述元素中只有N、S的最高价氧化物的水化物为强酸,Na的金属性最强,最高价氧化物的水化物碱性最强;
(2)电子层相同的离子,核电荷数越大半径越小;
(3)由①、④、⑤、三种元素H、O、Na形成的化合物是氢氧化钠;
(4)符合同一反应中两种单质对应元素既不同周期也不同主族的置换反应,如Mg置换C、Mg置换H;
(5)A、B、C含同一金属元素,X为强电解质,由图中连续反应可知,若A为铝盐,X为NaOH;若A为偏铝酸盐,X为强酸.
解答 解:由元素在周期表中的位置可知,①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是S,
(1)在上述元素的最高价氧化物对应的水化物中:属于强酸的是H2SO4、HNO3;碱性最强的是NaOH,
故答案为:H2SO4、HNO3;NaOH;
(2)电子层相同的离子,核电荷数越大半径越小,则离子半径为O2->Na+>Al3+,
故答案为:O2->Na+>Al3+;
(3)由①、④、⑤、三种元素H、O、Na形成的化合物是氢氧化钠,它是离子化合物,存在离子键和极性共价键,
故答案为:离子键、共价键;
(4)符合同一反应中两种单质对应元素既不同周期也不同主族的置换反应,如Mg置换C、Mg置换H,反应分别为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO、Mg+H2SO4=MgSO4+H2↑,
故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO、Mg+H2SO4=MgSO4+H2↑;
(5)A、B、C含同一金属元素,X为强电解质,由图中连续反应可知,若A为铝盐,X为NaOH;若A为偏铝酸盐,X为强酸(如H2SO4或HNO3)则B均为Al(OH)3,
对应的反应①的离子方程式为:Al3++3OH-=Al(OH)3↓或【Al(OH)4】-+H+=Al(OH)3↓+H2O,
故答案为:Al(OH)3;Al3++3OH-=Al(OH)3↓或【Al(OH)4】-+H+=Al(OH)3↓+H2O.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、元素化合物性质为解答的关键,侧重分析与应用能力的考查,注意元素周期律的应用,题目难度不.

 小学课时特训系列答案
小学课时特训系列答案| A. | 可逆反应 | B. | 任何反应 | C. | 溶液间反应 | D. | 气体间反应 |
| A. | 双氧水使酸性KMnO4溶液的红色褪去:3H2O2+2MnO4-+6H+=2Mn2++4O2↑+6H2O | |
| B. | HClO4的电离方程式:HClO4=H++ClO4- | |
| C. | 碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+OH-=CO32-+H2O | |
| D. | Fe2+被空气氧化:4Fe2++O2+2H2O=4Fe3++4OH- |
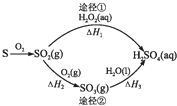
| A. | 已知S(l)+O2(g)═SO2(g)△H=-293.23kJ•mol-1,则S(s)+O2(g)═SO2(g)反应放出的热量小于293.23 kJ/mol | |
| B. | 含1 mol H2SO4的浓溶液与足量NaOH反应,放出的热量即为中和热 | |
| C. | 途径②中SO2和SO3均属于酸性氧化物 | |
| D. | 若△H1<△H2+△H3,则2H2O2(aq)═2H2O(l)+O2(g)为放热反应 |
| A. | 无色酚酞试液呈红色的溶液中:Na+、K+、SO42-、CO32- | |
| B. | 无色透明的溶液中:Cu2+、K+、SO42-、NO3- | |
| C. | 含有大量Ba(NO3)2的溶液中:Mg2+、NH4+、SO42-、Cl- | |
| D. | 紫色石蕊试液呈红色的溶液中:Ca2+、Cl-、Na+、HCO3- |
| A. | CO2的电子式为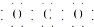 | B. | Cl-的结构示意图为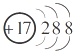 | ||
| C. | NaCl的电子式为Na+Cl- | D. | HCl的电子式为HCl |
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ⑨ | ④ | ⑤ | ⑩ | ⑥ | ⑦ | ⑧ |
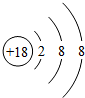 ;
;(2)表中金属性最强的元素是Na(用元素符号表示,下同),非金属性最强的元素是F,可作半导体材料的是Si元素的单质;
(3)表中能形成两性氢氧化物的元素是Al,写出该元素的单质与⑨的最高价氧化物的水化物反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
(4)⑨的最高价氧化物的水化物所含化学键类型离子键、共价键;
(5)①、⑥、⑦三种元素的最高价氧化物的水化物中酸性最强的是HClO4(填化学式);
(6)元素①的最高价氧化物的电子式
 ,④元素与⑦元素形成化合物的电子式
,④元素与⑦元素形成化合物的电子式 .
. 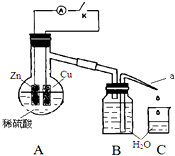 某同学分析Zn与稀H2SO4的反应.
某同学分析Zn与稀H2SO4的反应.(1)该反应的离子方程式是Zn+2H+=Zn2++H2↑.
(2)制H2时,用稀硫酸而不用浓硫酸,原因是浓H2SO4具有强氧化性,不能生成氢气.
(3)已知:Zn(s)+$\frac{1}{2}$O2(g)=ZnO(s)△H=-332kJ/mol
ZnO(s)+H2SO4(aq)=ZnSO4(aq)+H2O(l)△H=-112kJ/mol
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-286kJ/mol
则Zn与稀H2SO4反应生成1mol H2 时的反应热△H=-158kJ/mol.
(4)该同学用如图装置进行实验,分析影响反应速率的因素.
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
| 1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
①由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快(填“快”或“慢”),主要原因是形成原电池反应速度快.
②由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是溶液中的c(H+)大于闭合K时溶液中的c(H+).
③从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是断开K时,反应的化学能主要转化成热能,闭合K时,反应的化学能主要转化成电能,前者使溶液的温度升得更高,故反应速率更快.
| A. | NH3:0.002 mol•L-1•s-1 | B. | H2O:0.0015 mol•L-1•s-1 | ||
| C. | NO:0.0015 mol•L-1•s-1 | D. | O2:0.00125 mol•L-1•s-1 |