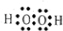题目内容
14.下列化学用语正确的是( )| A. | 双氧水使酸性KMnO4溶液的红色褪去:3H2O2+2MnO4-+6H+=2Mn2++4O2↑+6H2O | |
| B. | HClO4的电离方程式:HClO4=H++ClO4- | |
| C. | 碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+OH-=CO32-+H2O | |
| D. | Fe2+被空气氧化:4Fe2++O2+2H2O=4Fe3++4OH- |
分析 A.KMnO4具有氧化性,加入具有还原性的H2O2,两者发生氧化还原反应,紫色褪去,选项中电子不守恒;
B.强电解质为在溶液中能够完全电离,高氯酸属于强酸;
C.漏写铵根离子与碱的反应;
D.氢氧化铁为沉淀应写化学式.
解答 解:A.KMnO4与H2O2发生氧化还原反应,反应中MnO4-→Mn2+,Mn元素化合价由+7价→+2价,一个MnO4-得5个电子;H2O2→O2,O由-1价变成0价,一个H2O2分子失去2个电子,所以其最小公倍数为10,故MnO4-的计量数为2,双氧水的计量数为5,然后根据原子守恒配平其它元素,所以其离子方程式为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故A错误;B.电解质是指:在水溶液中或熔融状态下能够导电的化合物;强电解质是在水溶液中或熔融状态下,能完全电离的电解质,高氯酸属于强酸,其完全电离,电离方程式为:HClO4=H++ClO4-,故B正确;
C.碳酸氢铵溶液中加入过量氢氧化钠溶液的离子反应为NH4++HCO3-+2OH-═CO32-+H2O+NH3•H2O,故C错误;
D.Fe2+被空气氧化:12Fe2++3O2+6H2O=4Fe(OH)3↓+8Fe3+,故D错误;
故选B.
点评 本题考查离子反应方程式的书写,明确发生的化学反应是解答的关键,注意选项A中的氧化还原为解答的难点,题目难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
4.有关苯的结构和性质,下列说法正确的是( )
| A. | 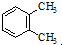 与 与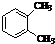 是同分异构体 是同分异构体 | |
| B. | 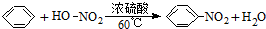 此反应是取代反应 此反应是取代反应 | |
| C. | 煤干馏得到的煤焦油可以分离出苯,苯是无色无味的液态烃 | |
| D. | 向2mL苯中加入1mL酸性高锰酸钾溶液,震荡后静置,可观察到液体分层,上层呈紫红色 |
5.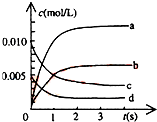 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)800℃,反应达到平衡时,NO的物质的量的浓度是0.0035mol/L;
(2)图中表示NO2的浓度变化曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是be.
a、v (NO2)=2v (O2)
b、容器内压强保持不变
c、v逆(NO)=v正(O2)
d、容器内混合气体的密度保持不变
e、该容器内颜色保持不变.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的浓度变化曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是be.
a、v (NO2)=2v (O2)
b、容器内压强保持不变
c、v逆(NO)=v正(O2)
d、容器内混合气体的密度保持不变
e、该容器内颜色保持不变.
9.医学上,科学家们设计以Pt和Zn为电极材料的电池,植入人体内作为心脏病患者的心脏起搏器的能源,它依靠人体内体液中存在的一定浓度的溶解的O2、H+、Zn2+进行工作.下列叙述正确的是( )
| A. | Pt为负极,Zn为正极 | |
| B. | Zn为负极,Pt为正极 | |
| C. | 负极反应式为Zn-2e-═Zn2+,正极反应式为2H++2e-═H2↑ | |
| D. | 负极反应式为Zn-2e-═Zn2+,正极反应式为O2+2H2O+4e-═4OH- |
2. 研究表明,化学反应的能量变化与反应物和生成物的键能有关.键能可以简单的理解为断开1mol 化学键时所需吸收的能量.下表是部分化学键的键能数据:
研究表明,化学反应的能量变化与反应物和生成物的键能有关.键能可以简单的理解为断开1mol 化学键时所需吸收的能量.下表是部分化学键的键能数据:
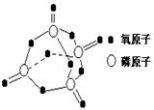
已知白磷的燃烧方程式为:P4(s)+5O2(g)=P4O10(s),该反应放出热量2378.0 kJ,且白磷分子结构为正四面体,4个磷原子分别位于正四面体的四个顶点,白磷完全燃烧的产物结构如右图所示,则上表中X为( )
 研究表明,化学反应的能量变化与反应物和生成物的键能有关.键能可以简单的理解为断开1mol 化学键时所需吸收的能量.下表是部分化学键的键能数据:
研究表明,化学反应的能量变化与反应物和生成物的键能有关.键能可以简单的理解为断开1mol 化学键时所需吸收的能量.下表是部分化学键的键能数据:已知白磷的燃烧方程式为:P4(s)+5O2(g)=P4O10(s),该反应放出热量2378.0 kJ,且白磷分子结构为正四面体,4个磷原子分别位于正四面体的四个顶点,白磷完全燃烧的产物结构如右图所示,则上表中X为( )
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ•mol-1 | 197 | 360 | 499 | X |
| A. | 434 | B. | 335 | C. | 237 | D. | 188 |
9.下列清洁剂能与常用的肥皂最为接近的是( )
| A. | CH3-(CH2)11C6H4-SO3Na | B. | CH3-(CH2)13-COOK | ||
| C. | CH3-(CH2)11-SO3Na | D. | CH3(CH2)nCH3(5≤n≤12) |
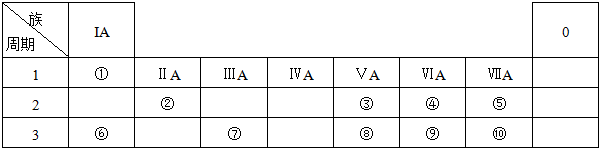
6.图为元素周期表的一部分,请根据元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)在上述元素的最高价氧化物对应的水化物中:属于强酸的是H2SO4、HNO3 (用化学式表示,下同);碱性最强的是NaOH.
(2)④、⑤、⑥的简单离子半径由大到小的顺序是O2->Na+>Al3+ (用离子符号表示).
(3)由①、④、⑤、三种元素组成的化合物中化学键的类型有:离子键、共价键.
(4)请写出涉及上述有关元素的两个置换反应(要求:同一反应中两种单质对应元素既不同周期也不同主族)2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO或Mg+H2SO4=MgSO4+H2↑;
(5)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:
A$→_{反应①}^{+X一定条件}$B$→_{反应②}^{+X一定条件}$C
若A、B、C含同一金属元素,X为强电解质,且反应都在溶液中进行.B的化学式为Al(OH)3.
对应的反应①的离子方程式为Al3++3OH-=Al(OH)3↓或【Al(OH)4】-+H+=Al(OH)3↓+H2O.
| 族 周期 | IA | 0 | ||||||
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)④、⑤、⑥的简单离子半径由大到小的顺序是O2->Na+>Al3+ (用离子符号表示).
(3)由①、④、⑤、三种元素组成的化合物中化学键的类型有:离子键、共价键.
(4)请写出涉及上述有关元素的两个置换反应(要求:同一反应中两种单质对应元素既不同周期也不同主族)2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO或Mg+H2SO4=MgSO4+H2↑;
(5)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:
A$→_{反应①}^{+X一定条件}$B$→_{反应②}^{+X一定条件}$C
若A、B、C含同一金属元素,X为强电解质,且反应都在溶液中进行.B的化学式为Al(OH)3.
对应的反应①的离子方程式为Al3++3OH-=Al(OH)3↓或【Al(OH)4】-+H+=Al(OH)3↓+H2O.