题目内容
13.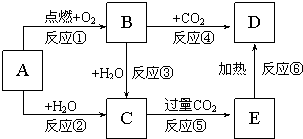 图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.它们的焰色反应均为黄色.请填写下列空白:
图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.它们的焰色反应均为黄色.请填写下列空白:(1)写出化学式:
ANa、BNa2O2、CNaOH、DNa2CO3.
(2)以上反应中属于氧化还原反应的有①②③④.(填写编号)
(3)写出A→C反应的离子方程式2Na+2H2O═2Na++2OH-+H2↑;E→D的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
分析 A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.它们的焰色反应均为黄色,则均为钠的单质或化合物,所以A为Na,结合转化关系可知,B为Na2O2,C为NaOH,D为Na2CO3,E为NaHCO3,然后结合单质及化合物的性质、化学用语来解答.
解答 解:A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.它们的焰色反应均为黄色,则均为钠的单质或化合物,所以A为Na,结合转化关系可知,B为Na2O2,C为NaOH,D为Na2CO3,E为NaHCO3,
(1)上述分析可知A为Na,B为Na2O2,C为NaOH,D为Na2CO3,E为NaHCO3,
故答案为:Na;Na2O2;NaOH;Na2CO3;
(2)以上反应中①为钠的燃烧,②为Na与水反应,③为过氧化钠与水反应,④为过氧化钠与二氧化碳反应,均属于氧化还原反应,⑤是二氧化碳和氢氧化钠溶液反应生成碳酸氢钠和水,⑥是碳酸氢钠分解生成碳酸钠、二氧化碳和水,⑤⑥不是氧化还原反应,
故答案为:①②③④;
(3)A-C反应②的离子反应为2Na+2H2O═2Na++2OH-+H2↑,E-D反应⑥为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,
故答案为:2Na+2H2O═2Na++2OH-+H2↑;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
点评 本题考查无机物的推断,明确焰色为黄色及A为单质为解答的突破口,熟悉钠及其化合物的性质是解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
3.下列各组物质,无氢气放出的是( )
| A. | 铝和氢氧化钠溶液 | B. | 镁和盐酸 | ||
| C. | Cu和稀硫酸 | D. | Si和NaOH溶液 |
4.下列有关胶体的叙述,不正确的是( )
| A. | 胶体区别于其他分散系的本质特征是分散质的微粒直径10-9m~10-7 m | |
| B. | 胶体在生物界普遍存在,应用也很广泛 | |
| C. | 用平行光照射氢氧化铁胶体产生一条光路,是由于光照使之发生分解生成氧化铁 | |
| D. | 氢氧化铁胶体净水是利用了胶体的吸附性 |
5.青蒿素(化学式为C15H22O5),熔点:156℃,无色针状晶体,水煎煮后分解而失效,主要用于间日疟、恶性疟的症状控制,下列关于青蒿素的说法中不正确的是( )
| A. | 青蒿素的摩尔质量是282 g/mol | |
| B. | 从植物黄花蒿茎叶中提取青蒿素可能会经过一系列复杂的变化 | |
| C. | 从题干信息推测,青蒿素应属于原子晶体 | |
| D. | 服用青蒿素治疗疟疾时,应用水在较低温度下溶解,以增强治疗功效 |
2.下列反应不属于氧化还原反应的是( )
| A. | 工业上利用电解饱和食盐水的产物制盐酸 | |
| B. | 工业上制备漂白粉 | |
| C. | 实验室制取氯气 | |
| D. | 炼铁工业上用石灰石除杂造渣 |
3.列措施对增大化学反应速率明显有效的是( )
| A. | Na与水反应时增大水的用量 | |
| B. | Fe与稀硫酸反应制取氢气时,改用浓硫酸 | |
| C. | 用H2O2制O2时加入MnO2 | |
| D. | 铝与盐酸反应时,加入稀的NaCl溶液 |


 太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.
太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.