题目内容
5.青蒿素(化学式为C15H22O5),熔点:156℃,无色针状晶体,水煎煮后分解而失效,主要用于间日疟、恶性疟的症状控制,下列关于青蒿素的说法中不正确的是( )| A. | 青蒿素的摩尔质量是282 g/mol | |
| B. | 从植物黄花蒿茎叶中提取青蒿素可能会经过一系列复杂的变化 | |
| C. | 从题干信息推测,青蒿素应属于原子晶体 | |
| D. | 服用青蒿素治疗疟疾时,应用水在较低温度下溶解,以增强治疗功效 |
分析 A.摩尔质量在数值上等于其相对分子质量,单位是g/mol;
B.从植物黄花蒿茎叶中提取青蒿素需要分离提纯;
C.分子晶体的熔沸点较低;
D.青蒿素(化学式为C15H22O5)熔点:156℃,高温下易分解.
解答 解:A.摩尔质量在数值上等于其相对分子质量,单位是g/mol,青蒿素的摩尔质量是282 g/mol,故A正确;
B.从植物黄花蒿茎叶中提取青蒿素需要分离提纯,所以需要经过一系列复杂的变化,故B正确;
C.分子晶体的熔沸点较低,该晶体的熔沸点较低,说明为分子晶体,故C错误;
D.青蒿素(化学式为C15H22O5)熔点:156℃,高温下易分解,所以服用青蒿素治疗疟疾时,应用水在较低温度下溶解,以增强治疗功效,故D正确;
故选C.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生获取信息、利用信息解答问题能力,正确获取信息并解答问题是解本题关键,题目难度不大.

练习册系列答案
相关题目
15.下列叙述正确的是( )
| A. | 常温常压下,1.5 mol NO2的体积约为33.6 L | |
| B. | NaOH的摩尔质量是40 g | |
| C. | 100 mL水中溶解了8.4 g NaHCO3,则溶液中Na+的物质的量浓度为1 mol/L | |
| D. | 同温同压下,相同体积的C12和SO2气体所含的分子数一定相同 |
20.关于炼铁原理下列说法正确的是( )
| A. | 铁矿石在高温下被氧化成铁 | B. | 生铁中杂质被氧化 | ||
| C. | 铁矿石在高温下被焦炭还原成铁 | D. | 铁矿石在高温下被CO还原成铁 |
10.关于溴和碘的说法中不合理的是( )
| A. | 单质溴是一种红棕色液体 | B. | 溴水可使湿润的淀粉KI试纸变蓝 | ||
| C. | 单质碘易升华 | D. | 碘单质是从海水中大量提取的 |
14.某溶液与Al反应能放出H2,下列离子在该溶液中一定能大量共存的是( )
| A. | K+、Fe2+、Cl-、SO42- | B. | Na+、K+、Cl-、SO42- | ||
| C. | Mg2+、K+、H+、SO42- | D. | K+、Ca2+、HCO3-、Cl- |
15.下列物质的名称、化学式、所属类别对应正确的是( )
| A. | 石英 SiO2 酸 | B. | 纯碱 Na2CO3 碱 | ||
| C. | 绿矾 FeSO4•7H2O 盐 | D. | 磁铁矿 Fe2O3 金属氧化物 |
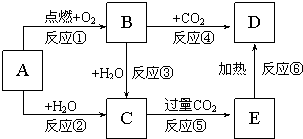 图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.它们的焰色反应均为黄色.请填写下列空白:
图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.它们的焰色反应均为黄色.请填写下列空白: