题目内容
15.有关电化学说法错误的是( )| A. | 1 mol H2和0.5 mol O2反应放出的热量就是H2的燃烧热 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,相同条件下,前者放出的热量多 | |
| C. | 水中的钢闸门连接电源的负极,属于外加电流的阴极保护法 | |
| D. | 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀 |
分析 A.氢气的燃烧热是1mol氢气燃烧生成1mol液态水时放出的热量;
B.等质量的同种物质,气态时具有的能量高;
C.与负极相连作阴极,阴极被保护;
D.铁遇浓硝酸会在铁的表面形成致密的氧化膜.
解答 解:A.氢气的燃烧热是1mol氢气燃烧生成1mol液态水时放出的热量,没有说明生成物水的状态,所以不一定是燃烧热,故A错误;
B.等质量的硫蒸气和硫固体,硫蒸气具有的能量高,所以分别完全燃烧,相同条件下,前者放出的热量多,故B正确;
C.水中的钢闸门连接电源的负极,钢闸作阴极,阴极被保护,属于外加电流的阴极保护法,故C正确;
D.铁遇浓硝酸会在铁的表面形成致密的氧化膜,可保护内部不被腐蚀,故D正确.
故选A.
点评 本题考查了燃烧热、物质状态与能量的关系、金属的电化学防护、铁的性质,题目难度不大,注意相关知识的积累,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
3.某物质中可能有甲酸、乙酸、甲醇和甲酸乙酯1种物质中1种或几种,在鉴别时有下列现象:(1)有银镜反应;(2)加入新制Cu(OH)2悬浊液沉淀不溶解;(3)与含酚酞的NaOH溶液共热发现溶液中红色逐渐消失以至无色,下列叙述正确的有( )
| A. | 几种物质都有 | B. | 有甲酸乙酯,可能有甲酸 | ||
| C. | 有甲酸乙酯和甲醇 | D. | 有甲酸乙酯,可能有甲醇 |
10.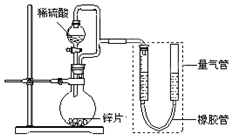 某同学设计了如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.
某同学设计了如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.
请回答:
(1)用上述装置探究影响化学反应速率的因素.
①圆底烧瓶中发生反应的离子方程式是Zn+2H+=Zn2++H2↑.
②用上述装置进行实验,以生成9.0mL气体为计时终点,结果为t1>t2
比较实验Ⅰ和Ⅱ可以得出的实验结论是在其它条件一定时,化学反应速率随反应物浓度的增大而增大.
③若将锌片换成含杂质的粗锌片,且控制其他条件使其与上述实验完全一致,所测得的反应速率均大于上述实验对应的数据.粗锌片中所含杂质可能是abc(填序号).
a.石墨 b.银 c.铜 d.沙粒(二氧化硅)
(2)用上述装置测定粗锌片的纯度.
①连接好装置,检查装置气密性,称量粗锌片mg置于圆底烧瓶中,滴加足量稀硫酸,充分反应直至不再产生气体为止,测得气体体积为VL,则粗锌片的纯度为$\frac{65V}{22.4m}$×100%.
②本实验在读数前对量气管的操作是调整左右两管的液面高度相平,且视线与液面相平.
③本套装置中若考虑滴入的稀硫酸的体积(假设其它操作都正确),则测得的气体的体积将.无影响(填“偏大”、“偏小”或“无影响”,)
(3)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀.
①圆底烧瓶中的试剂可选用c(填序号).
NH4Cl溶液 b.C2H5OH c.Na2CO3溶液 d.稀硫酸
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是量气管右端液面下降,左端液面上升.
 某同学设计了如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.
某同学设计了如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.请回答:
(1)用上述装置探究影响化学反应速率的因素.
①圆底烧瓶中发生反应的离子方程式是Zn+2H+=Zn2++H2↑.
②用上述装置进行实验,以生成9.0mL气体为计时终点,结果为t1>t2
| 序号 | V(H2SO4)/mL | c(H2SO4)/mol•L-1 | t/s |
| Ⅰ | 40 | 1 | t1 |
| Ⅱ | 40 | 4 | t2 |
③若将锌片换成含杂质的粗锌片,且控制其他条件使其与上述实验完全一致,所测得的反应速率均大于上述实验对应的数据.粗锌片中所含杂质可能是abc(填序号).
a.石墨 b.银 c.铜 d.沙粒(二氧化硅)
(2)用上述装置测定粗锌片的纯度.
①连接好装置,检查装置气密性,称量粗锌片mg置于圆底烧瓶中,滴加足量稀硫酸,充分反应直至不再产生气体为止,测得气体体积为VL,则粗锌片的纯度为$\frac{65V}{22.4m}$×100%.
②本实验在读数前对量气管的操作是调整左右两管的液面高度相平,且视线与液面相平.
③本套装置中若考虑滴入的稀硫酸的体积(假设其它操作都正确),则测得的气体的体积将.无影响(填“偏大”、“偏小”或“无影响”,)
(3)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀.
①圆底烧瓶中的试剂可选用c(填序号).
NH4Cl溶液 b.C2H5OH c.Na2CO3溶液 d.稀硫酸
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是量气管右端液面下降,左端液面上升.
20.下列热化学方程式中的反应热下划线处表示燃烧热的是( )
| A. | 4NH3(g)+5O2(g)═4 NO(g)+6 H2O(g)△H=+a kJ•mol-1 | |
| B. | C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H=-b kJ•mol-1 | |
| C. | 2CO(g)+O2(g)═2CO2(g)△H=-c kJ•mol-1 | |
| D. | CH3CH2OH(l)+$\frac{1}{2}$O2(g)═CH3CHO(l)+H2O(g)△H=-d kJ•mol-1 |
5.核素${\;}_{92}^{238}$U中子数与质子数之差是( )
| A. | 54 | B. | 92 | C. | 146 | D. | 238 |
 2c(g) ΔH1<0
2c(g) ΔH1<0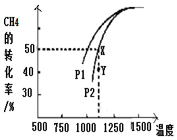 研究含氮、硫污染物的治理是环保的一项重要工作.
研究含氮、硫污染物的治理是环保的一项重要工作.