题目内容
4.阿伏伽德罗常数约为6.02×1023mol-1,下列叙述中正确的是( )①1.01×105Pa、25℃时,2.24LCl2中含有的原子数为0.2NA
②0.1L3mol•L-1NH4NO3溶液中含有的N原子数目为0.3NA
③5.6g铁粉和足量的硫酸铜溶液反应生成的铜原子数为NA
④常温常压下,46gNO2和N2O4的混合物中含有的原子数为3NA
⑤1molNH3所含有的电子数为17NA
⑥1mol/LNaCl溶液中所含的Na+数为NA
⑦常温常压下,28g氮气所含的原子数为2NA
⑧标准状况下,22.4L水所含有的分子数目为NA.
| A. | ①④⑤ | B. | ②③⑥⑦ | C. | ④⑦ | D. | ⑤⑥ |
分析 ①1.01×105Pa、25℃时,气体摩尔体积大于22.4L/mol;
②求出0.1L3mol•L-1NH4NO3溶液中含有的硝酸铵的物质的量,然后根据硝酸铵中含2个氮原子来分析;
③求出5.6g铁粉的物质的量,然后根据1mol铁粉能置换出1mol单质铜来分析;
④NO2和N2O4的最简式均为NO2;
⑤氨气为10电子分子;
⑥溶液体积不明确;
⑦求出28g氮气的物质的量,然后根据氮气为双原子分子来分析;
⑧标准状况下,水为液体.
解答 解:①1.01×105Pa、25℃时,气体摩尔体积大于22.4L/mol,故2.24L氯气的物质的量小于0.1mol,则原子个数小于0.2NA个,故错误;
②0.1L3mol•L-1NH4NO3溶液中含有的硝酸铵的物质的量n=3mol/L×0.1L=0.3mol,而硝酸铵中含2个氮原子,故0.3mol硝酸铵中含0.6mol氮原子即0.6NA个,故错误;
③5.6g铁粉的物质的量为0.1mol,而1mol铁粉能置换出1mol单质铜,故0.1mol铁粉能置换出0.1mol铜,故得到的铜原子的个数为0.1NA个,故错误;
④NO2和N2O4的最简式均为NO2,故46gNO2和N2O4的混合物中含有的NO2的物质的量为1mol,故含3mol即3NA个原子,故正确;
⑤氨气为10电子分子,故1mol氨气中含10NA个电子,故错误;
⑥溶液体积不明确,故溶液中的钠离子的个数无法计算,故错误;
⑦28g氮气的物质的量为1mol,而氮气为双原子分子,故1mol氮气中含2mol原子即2NA个,故正确;
⑧标准状况下,水为液体,故不能根据气体摩尔体积来计算其物质的量,故错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

| A. | 1 mol H2和0.5 mol O2反应放出的热量就是H2的燃烧热 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,相同条件下,前者放出的热量多 | |
| C. | 水中的钢闸门连接电源的负极,属于外加电流的阴极保护法 | |
| D. | 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀 |
| A. | 铁在熔融状态下能导电,所以铁是电解质 | |
| B. | 氯化氢在熔融状态下不导电,所以氯化氢是非电解质 | |
| C. | 氯气的水溶液能导电,所以氯气是电解质 | |
| D. | 电解质和非电解质都是纯净物 |
| 选项 | 操作 | 现象 | 解释、结论 |
| A | 长期露置于潮湿空气中的Fe粉中加入足量的稀盐酸充分反应,滴入KSCN溶液 | 溶液呈红色 | 稀盐酸将Fe氧化为Fe3+ |
| B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了Na2CO3晶体 |
| C | Al箔插入浓硝酸中 | 无现象 | Al在浓硝酸中钝化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到蓝色石蕊试纸上 | 试纸变红色 | 浓氨水呈碱性 |
| A. | A | B. | B | C. | C | D. | D |
| A. | C | B. | Si | C. | S | D. | Cl |
| A. | ⅣA族元素氢化物沸点:SiH4>CH4,所以ⅤA族元素氢化物沸点:PH3>NH3 | |
| B. | 第二周期元素氢化物稳定性:HF>H2O,第三周期元素氢化物稳定性:HCl>H2S | |
| C. | ⅦA族元素的非金属性:F>Cl,所以ⅦA族元素氢化物的酸性:HF<HCl | |
| D. | 镁比铝活泼,工业上用电解熔融氧化铝制铝,所以工业上也用电解熔融氧化镁制镁 |
| A. | 二溴乙烷:CH2BrCH2Br | B. | 3-乙基-1-丁烯: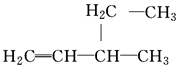 | ||
| C. | 2-甲基-2,4-己二烯: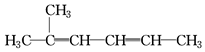 | D. | 2,2,3-三甲基戊烷: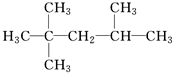 |
| A. | 盐酸 | B. | 氢氧化钠溶液 | C. | 溴水 | D. | 新制氢氧化铜 |
 氨水,溶液的导电性增强
氨水,溶液的导电性增强