题目内容
19.下列操作或装置能达到实验目的是( )| A. | 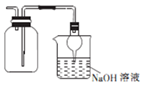 收集NO2并防止其污染环境 | |
| B. | 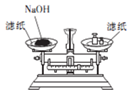 称取一定量的NaOH | |
| C. | 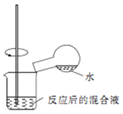 检验浓硫酸与铜反应后的产物中,是否含有铜离子 | |
| D. | 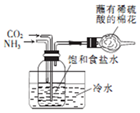 制取NaHCO3 |
分析 A.二氧化氮密度比空气大,应用向上排空法收集;
B.NaOH潮解,具有腐蚀性;
C.稀释酸液,应避免酸液飞溅;
D.NaCl、氨气、二氧化碳反应生成碳酸氢钠和氯化铵.
解答 解:A.二氧化氮的密度比空气密度大,则图中导管应长进,故A错误;
B.NaOH潮解,具有腐蚀性,应在左盘小烧杯中称量,故B错误;
C.稀释时将密度大的液体注入密度小的液体中,试剂的顺序不合理,故C错误;
D.NaCl、氨气、二氧化碳反应生成碳酸氢钠和氯化铵,图中装置可制备碳酸氢钠,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握图中实验装置的作用、物质的制备、气体的收集、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.常温下,甲酸、乙酸电离常数:Ka(HCOOH)=1.77x10-4、Ka(CH3COOH)=1.75×10-5有甲、乙、丙三种溶液:
下列叙述错误的是( )
| 甲 | 1000mL 0.1mol/L HCOONa溶液 |
| 乙 | 1000mL 0.1mol/L CH3COONa溶液 |
| 丙 | 1000mL含HCOONa、CH3COONa各0.05mol的溶液 |
| A. | 溶液中c(Na+):甲=乙>丙 | |
| B. | 溶液中阴、阳离子和酸分子总数:甲<丙<乙 | |
| C. | 溶液pH:甲<丙<乙 | |
| D. | 溶液中阴、阳离子总数:甲>丙>乙 |
14.某有机物的结构简式为 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 该物质的分子式为C11H10O3 | |
| B. | 该有机物含有4种官能团 | |
| C. | 1 mol该有机物最多可以消耗2 mol NaOH | |
| D. | 该有机物不能发生消去反应 |
4.图中没有涉及到的能量转化形式是( )


| A. | 化学能转化为热能 | B. | 太阳能转化为化学能 | ||
| C. | 势能转化为电能 | D. | 化学能转化为势能 |
11.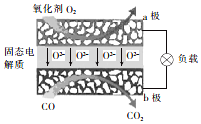 为体现节能减排的理念,中国研制出了新型固态氧化物燃料电池(SOFC),该电池的丁作原理如图所示.下列说法正确的是( )
为体现节能减排的理念,中国研制出了新型固态氧化物燃料电池(SOFC),该电池的丁作原理如图所示.下列说法正确的是( )
 为体现节能减排的理念,中国研制出了新型固态氧化物燃料电池(SOFC),该电池的丁作原理如图所示.下列说法正确的是( )
为体现节能减排的理念,中国研制出了新型固态氧化物燃料电池(SOFC),该电池的丁作原理如图所示.下列说法正确的是( )| A. | 电子从b极经导线流向a极 | |
| B. | 正极的电极反应式为O2+4e-+2H2O═4OH- | |
| C. | 还可以选用NaOH固体作固态电解质 | |
| D. | 若反应中转移1 mol电子,则生成22.4L(标准状况)CO2 |
8.“漆器”是中国古代在化学工艺及工艺美术方面的重要发明,所用生漆是从我国特产漆树割取的天然液汁.生漆主要成分是漆酚  ,-C15H27为链烃基,则漆酚不应具有的化学性质是( )
,-C15H27为链烃基,则漆酚不应具有的化学性质是( )
 ,-C15H27为链烃基,则漆酚不应具有的化学性质是( )
,-C15H27为链烃基,则漆酚不应具有的化学性质是( )| A. | 可以跟FeCl3溶液发生显色反应 | B. | 可以使酸性KMnO4溶液褪色 | ||
| C. | 可以跟Na2CO3溶液反应放出CO2 | D. | 可以发生取代反应和加成反应 |
9.根据图,下列判断中正确的是( )
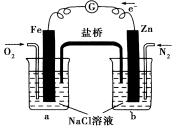

| A. | 烧杯b中发生还原反应 | |
| B. | 烧杯b中发生的反应为2Cl--2e-═Cl2↑ | |
| C. | 烧杯a中发生的反应为2H++2e-═H2↑ | |
| D. | 烧杯a中的溶液pH升高 |
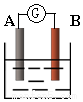 如图为原电池装置示意图:
如图为原电池装置示意图: