题目内容
10.A的分子式为C8H16O2,可发生如下转化: ,其中B与E互为同分异构体,则A可能的结构有( )
,其中B与E互为同分异构体,则A可能的结构有( )| A. | 2种 | B. | 6种 | C. | 8种 | D. | 4种 |
分析 分子式为C8H16O2的有机物A,它能在酸性条件下水解生成B和C,说明有机物A为酯,根据分子组成可知应为饱和一元酸和饱和一元醇形成的酯,能在酸性条件下水解生成B和C,C能经两步氧化得E,则C为醇,C中与羟基所连碳上有2个氢原子,B为羧酸,其中B与E互为同分异构体,则B、C中各有4个碳原子,则以此解答该题.
解答 解:分子式为C8H16O2的有机物A,它能在酸性条件下水解生成B和C,说明有机物A为酯,根据分子组成可知应为饱和一元酸和饱和一元醇形成的酯,能在酸性条件下水解生成B和C,C能经两步氧化得E,则C为醇,C中与羟基所连碳上有2个氢原子,B为羧酸,其中B与E互为同分异构体,则B、C中各有4个碳原子,B可能的结构为CH3CH2CH2COOH、(CH3)2CHCOOH,C可能的结构为CH3CH2CH2CH2OH、(CH3)2CHCH2OH,所以A可能的结构为(CH3)2CHCOOCH2CH2CH2CH3、CH3CH2CH2COOCH2CH(CH3)2,共2种,
故选D.
点评 本题考查有机物的推断,侧重于学生的分析能力的考查,为高频考点,题目难度中等,B与E互为同分异构体且为同类物质,说明B和E的碳原子数相同,但碳链不相同.

练习册系列答案
相关题目
15.青蒿素是一种有效的抗疟药.常温下,青蒿素为无色针状晶体,难溶于水,易溶于有机溶剂,熔点为156~157℃.提取青蒿素的方法之一是乙醚浸取法,提取流程如图1:
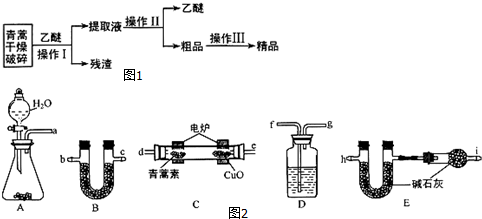
请回答下列问题:
(1)对青蒿进行破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率.
(2)操作Ⅰ用到的玻璃仪器是漏斗、玻璃棒、烧杯,操作Ⅱ的名称是蒸馏.
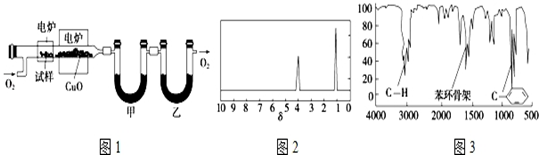
(3)用如图2的实验装置测定青蒿素的化学式,将28.2g青蒿素放在燃烧管C中充分燃烧:
①仪器各接口的连接顺序从左到右依次为afgdebchi(每个装置限用一次).
②装置C中CuO的作用是使青蒿素充分氧化生成CO2和H2O.
③装置D中的试剂为浓硫酸.
④已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验,测量数据如表:
则青蒿素的最简式为C15H22O5.
(4)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,与青蒿素化学性质相似的物质是C(填字母代号).
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖.

请回答下列问题:
(1)对青蒿进行破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率.
(2)操作Ⅰ用到的玻璃仪器是漏斗、玻璃棒、烧杯,操作Ⅱ的名称是蒸馏.
(3)用如图2的实验装置测定青蒿素的化学式,将28.2g青蒿素放在燃烧管C中充分燃烧:
①仪器各接口的连接顺序从左到右依次为afgdebchi(每个装置限用一次).
②装置C中CuO的作用是使青蒿素充分氧化生成CO2和H2O.
③装置D中的试剂为浓硫酸.
④已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验,测量数据如表:
| 装置质量 | 实验前/g | 实验后/g |
| B | 22.6 | 42.4 |
| E(不含干燥管) | 80.2 | 146.2 |
(4)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,与青蒿素化学性质相似的物质是C(填字母代号).
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖.
1.某化学学习小组的同学对放置已久的过氧化钠的成分进行探究,请回答下列问题:
(1)反应2Na2O2+2H2O═4NaOH+O2↑的还原剂是Na2O2(写化学式);反应2Na2O2+2CO2═2Na2CO3+O2的氧化剂是Na2O2(写化学式),每生成1mol O2转移2mol电子.
(2)进行探究:
①提出假设.
假设1:全部是Na2O2
假设2:全部是Na2CO3
假设3:是Na2O2与Na2CO3的混合物.
②设计方案,进行实验.请写出实验步骤以及预期的现象和结论(可不填满).限选实验试剂和仪器:蒸馏水、1mol•L-1 H2SO4溶液、澄清石灰水、淀粉-KI溶液、酚酞溶液、火柴、试管、小烧杯、胶头滴管.
(1)反应2Na2O2+2H2O═4NaOH+O2↑的还原剂是Na2O2(写化学式);反应2Na2O2+2CO2═2Na2CO3+O2的氧化剂是Na2O2(写化学式),每生成1mol O2转移2mol电子.
(2)进行探究:
①提出假设.
假设1:全部是Na2O2
假设2:全部是Na2CO3
假设3:是Na2O2与Na2CO3的混合物.
②设计方案,进行实验.请写出实验步骤以及预期的现象和结论(可不填满).限选实验试剂和仪器:蒸馏水、1mol•L-1 H2SO4溶液、澄清石灰水、淀粉-KI溶液、酚酞溶液、火柴、试管、小烧杯、胶头滴管.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中,滴加足量1mol•L-1 H2SO4溶液,然后将内壁附有澄清石灰水的烧杯罩于试管口 | 若澄清石灰水未见浑浊,则假设1成立;若澄清石灰水变浑浊,则假设2或假设3成立 或假设1不成立. |
| 步骤2: | |
| 步骤3: |
5.表为元素周期表的一部分,请参照元素①~⑩在表中的位置,用化学用语回答下列问题:
(1)⑦为O(填元素符号);
(2)①、③、⑤的最高价最高价氧化物对应的水化物中,碱性最强的是NaOH (填化学式);
(3)②、③、④三种元素可形成的离子,离子半径由大到小的顺序为K+>Ca2+>Mg2+(请填离子符号);
(4)①和⑨两元素形成化合物灼烧时的焰色为黄 色;该化合物的溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=2Cl-+Br2.
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①、③、⑤的最高价最高价氧化物对应的水化物中,碱性最强的是NaOH (填化学式);
(3)②、③、④三种元素可形成的离子,离子半径由大到小的顺序为K+>Ca2+>Mg2+(请填离子符号);
(4)①和⑨两元素形成化合物灼烧时的焰色为黄 色;该化合物的溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=2Cl-+Br2.
19.下列说法不正确的是( )
| A. | pH=7的溶液不一定是中性溶液 | |
| B. | 0.2 mol•L-1的盐酸与等体积水混合后pH=1(体积变化忽略不计) | |
| C. | 能自发进行的化学反应,一定是△H<0、△S>0 | |
| D. | NaNO2固体溶于水会促进水的电离(已知Ka(HNO2)=4.6×10-4) |
 一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
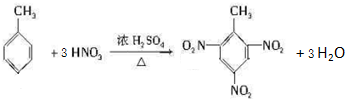 .
.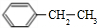 、
、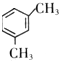 .
.