题目内容
2.下列除杂试剂或操作方法不正确的是( )| 序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
| ① | NaCl | BaCl2 | 加入过量的K2CO3溶液,过滤,再加适量的盐酸并加热 |
| ② | FeSO4溶液 | CuSO4 | 加入过量Fe粉,过滤 |
| ③ | CO2 | HCl | 通过盛饱和Na2CO3溶液洗气瓶,再通过盛H2SO4洗气瓶 |
| ④ | 自来水 | 植物油 | 萃取分液 |
| A. | ①④ | B. | ②③ | C. | ①③④ | D. | ①②④ |
分析 ①氯化钡与碳酸钾反应生成沉淀和KCl;
②Fe与硫酸铜反应生成硫酸亚铁和Cu;
③二者均与Na2CO3溶液反应;
④自来水与植物油分层.
解答 解:①氯化钡与碳酸钾反应生成沉淀和KCl,引入新杂质,不能除杂,应选适量碳酸钠,故错误;
②Fe与硫酸铜反应生成硫酸亚铁和Cu,反应后过滤可除杂,故正确;
③二者均与Na2CO3溶液反应,不能除杂,应选饱和碳酸氢钠溶液洗气瓶,再通过盛H2SO4洗气瓶,故错误;
④自来水与植物油分层,直接分液可分离,不需要萃取,故错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、混合物分离提纯、实验操作为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
1.用一种阴、阳离子双隔膜三室电解槽处理废水中的NH4+,模拟装置如图所示.下列说法不正确的是( )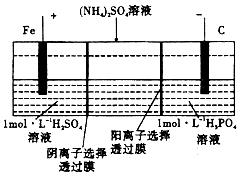

| A. | 阳极室溶液由无色变成浅绿色 | |
| B. | 当电路中通过lmol电子的电量时,阴极有0.5mol的气体生成 | |
| C. | 电解时中间室(NH4)2SO4溶液浓度下降 | |
| D. | 电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4 |
2.两种气态烃的混合物共2.24L(标准状况下),完全燃烧后得3.36L(标准状况下)二氧化碳和3.6g的水.下列说法中,正确的是( )
| A. | 混合气体中一定含有甲烷 | B. | 混合气体中一定含有乙烯 | ||
| C. | 混合气体中一定含有甲烷和乙烯 | D. | 混合气体中一定含有乙烷 |
10.在2L的密闭容器中发生如下反应:3A+B=C+D,若开始时加入的A和B均是4mol,在前10s内A的平均反应速率为0.12mol/(L•S),则10S时容器内C的物质的量为( )
| A. | 3.2mol | B. | 2.4mol | C. | 0.8mol | D. | 0.4mol |
7.实验室测得4molSO2参加下述反应:已知2SO2(g)+O2(g)?2SO3(g);△H=-197kJ•mol-1,当放出314.3kJ热量时,SO2的转化率最接近于( )
| A. | 40% | B. | 50% | C. | 80% | D. | 90% |
11.下列有关化学反应方向及其判据的说法中错误的是( )
| A. | 1 mol H2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)] | |
| B. | 凡是放热反应都是自发的,因为吸热反应都是非自发的 | |
| C. | CaCO3(s)?CaO(s)+CO2(g)△H>0 能否自发进行与温度有关 | |
| D. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
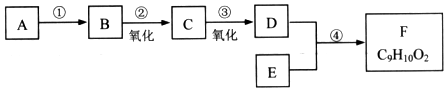
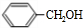 ;
;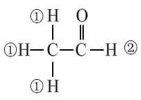 已知化合物分子结构中的等效氢原子(在化合物的结构中所处的环境相同的H原子)在核磁共振氢谱(1HNMR)中会给出相同的峰(信号),峰的强度与H原子数成正比.例如:乙醛的结构中有①②两类氢原子且个数比为3:1,它在1HNMR谱中也有2个信号峰,其强度之比为3:l.
已知化合物分子结构中的等效氢原子(在化合物的结构中所处的环境相同的H原子)在核磁共振氢谱(1HNMR)中会给出相同的峰(信号),峰的强度与H原子数成正比.例如:乙醛的结构中有①②两类氢原子且个数比为3:1,它在1HNMR谱中也有2个信号峰,其强度之比为3:l.