题目内容
12.下列有关物质的性质与用途都正确且具有对应关系的是( )| A. | NH4HCO3受热易分解,可用作氮肥 | |
| B. | Na2CO3具有碱性,可用作胃酸中和剂 | |
| C. | SiO2易传导光信号,可用作光导纤维 | |
| D. | Ca(ClO)2在空气中不稳定,可用于漂白纸张 |
分析 A.铵盐易分解产生氨气、水、二氧化碳,氮元素损失;
B.用作胃酸中和剂的是碱性更弱的碳酸氢钠;
C.二氧化硅易传导光信号,可用作光导纤维;
D.漂白纸张是利用了次氯酸的强氧化性.
解答 解:A.铵盐受热分解产生氨气、水、二氧化碳,氮元素损失,碳酸氢铵用作氮肥是土壤吸收铵根利用氮元素,故A错误;
B.碳酸钠水解呈碱性,但碱性较强,用作胃酸中和剂的是碱性更弱的碳酸氢钠,故B错误;
C.二氧化硅易传导光信号,可用作光导纤维,故C正确;
D.在空气中次氯酸钙与二氧化碳、水反应生成次氯酸,是次氯酸具有强氧化性而漂白纸张,故D错误;
故选C.
点评 本题考查常见物质的性质和用途,题目难度不大,明确物质的性质决定用途,学习中注意相关基础知识的积累.

练习册系列答案
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
2.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素B的化合物可以用来做焰火材料 | |
| B. | 化合物AE与CE含有相同类型的化学键 | |
| C. | 工业上常用电解法制备元素C、D、E的单质 | |
| D. | 元素B、D的最高价氧化物对应的水化物之间可能发生反应 |
3.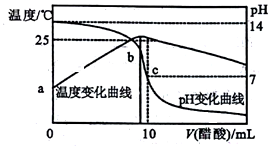 在某温度时,将nmol•L-1醋酸溶液滴入10mL1.0mol•L-1NaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )
在某温度时,将nmol•L-1醋酸溶液滴入10mL1.0mol•L-1NaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )
 在某温度时,将nmol•L-1醋酸溶液滴入10mL1.0mol•L-1NaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )
在某温度时,将nmol•L-1醋酸溶液滴入10mL1.0mol•L-1NaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )| A. | 水的电离程度:c>b | B. | a点Kw比b点大 | ||
| C. | n>1.0 | D. | c点:Ka(CH3COOH)=$\frac{10}{10n+1}$×10-8 |
20.利用实验器材(规格和数量不限),能够完成相应实验的一项是( )
| 选项 | 实验器材(省略夹持装置) | 相应实验 |
| A | 量筒、温度计、烧杯、碎纸条、盖板 | 中和热的测定 |
| B | 烧杯、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
| C | 量筒、玻璃捧、烧杯、100mL容量瓶 | 用浓盐酸配制100mL 0.1mol•L-1的稀盐酸溶液 |
| D | 烧杯、酸式滴定管、碱式滴定管 | 用出H2SO4标准液滴定未知浓度的NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
7.元素①~⑩在周期表中的位置如表所示,试回答下列问题.
(1)上述10种元素中,化学性质最不活泼的是Ar(填元素符号,下同);与水反应最激烈的金属元素是K.
(2)元素 ②的气态氢化物的分子式是NH3;上述10种元素中,其最高价氧化物对应水化物的酸性最强的物质是HClO4(填化学式).
(3)用电子式表示元素③与④形成1:2型化合物的形成过程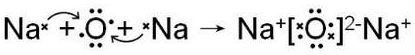 .
.
(4)①②⑤元素的原子半径由小到大的顺序为N、C、Mg(用元素符号表示);③⑦⑩元素的气态氢化物的稳定性由强到弱的顺序为H2O、HCl、HBr(用氢化物的化学式表示).
(5)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)元素 ②的气态氢化物的分子式是NH3;上述10种元素中,其最高价氧化物对应水化物的酸性最强的物质是HClO4(填化学式).
(3)用电子式表示元素③与④形成1:2型化合物的形成过程
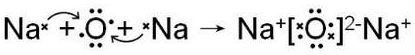 .
.(4)①②⑤元素的原子半径由小到大的顺序为N、C、Mg(用元素符号表示);③⑦⑩元素的气态氢化物的稳定性由强到弱的顺序为H2O、HCl、HBr(用氢化物的化学式表示).
(5)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
17.能正确表示下列反应的离子方程式的是( )
| A. | Na2S2O3溶液与H2SO4溶液混合:S2O32-+4H+═SO42-+S↓+2H2O | |
| B. | 硝酸银溶液中滴入少量氨水:Ag++2NH2•H2O═[Ag(NH3)2]++2H2O | |
| C. | AgI悬浊液中滴入适量Na2S溶液:2AgI+S2-═Ag2S+2I- | |
| D. | Fe(SCN)3溶液中滴入几滴0.01mol/LNaOH溶液:Fe3++3OH-═Fe(OH)3↓ |
4.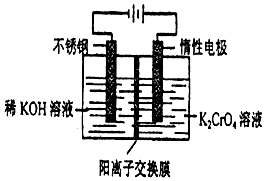 以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )
以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )
 以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )
以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )| A. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动 | |
| B. | 在阴极室,通电后KOH溶液不断变浓,并产生气体H2 | |
| C. | CrO42-通过离子交换膜从阳极区域迁移到阴极区域 | |
| D. | 电解一段时间后测定阳极液中K和Cr的物质的量之比为d,则导线中转移电子的物质的量为(2-d)mol |
13.25℃时,下列有关电解质溶液的说法正确的是( )
| A. | 将Na2CO3溶液用水稀释后,pH变大,Kw不变 | |
| B. | 向有AgCl固体的饱和溶液中加少许水,c(Ag+)和Ksp(AgCl)都不变 | |
| C. | pH=4.75浓度均为0.1mol/L的CH3COOH、CH3COONa的混合溶液中:c(CH3COO-)+c(OH-)<c(H+)+c(CH3COOH) | |
| D. | 分别用pH=2和pH=3的CH3COOH溶液中和等物质的量的NaOH,消耗CH3COOH溶液的体积分别为Va和Vb,则10Va>Vb |
14.下列有关化学用语表示正确的是( )
| A. | 中子数为14的铝原子:${\;}_{13}^{14}$Al | B. | 次氯酸的电子式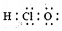 | ||
| C. | O2-的结构示意图: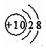 | D. | 聚四氟乙烯的结构简式: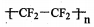 |