题目内容
6.下列溶液中不存在配离子的是( )| A. | CuSO4水溶液 | B. | 银氨溶液 | C. | 硫氰化铁溶液 | D. | I2的CCl4溶液 |
分析 配离子是由一个金属阳离子和一定数目的中性分子或阴离子以配位键结合而成的复杂离子,可能存在于配位化合物晶体中,也可能存在于溶液中,据此解答.
解答 解:A.水对铜离子有络合作用,CuSO4水溶液中存在四水合铜络离子,铜离子提供空轨道,水分子提供孤对电子,存在配离子,故A不选;
B.银氨溶液中银离子提供空轨道,氨气提供孤对电子,存在配离子,故B不选;
C.硫氰化铁溶液中铁离子提供空轨道,硫氰根离子提供孤对电子,存在配离子,故C不选;
D.I2的CCl4溶液为碘单质的四氯化碳溶液,无配离子,故D选;
故选D.
点评 本题考查配离子,题目难度中等,注意配离子可能存在于配位化合物晶体中,也可能存在于溶液中,把握相关概念是解答的关键.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案
相关题目
16.在冷的浓硝酸中,下列金属最难溶解的是( )
| A. | 银 | B. | 镁 | C. | 铝 | D. | 铜 |
17.如图实验操作正确的是( )
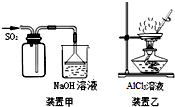

| A. | 用装置甲收集SO2 | |
| B. | 用装置乙制备AlCl3晶体 | |
| C. | 中和滴定时,锥形瓶用待装液润洗 | |
| D. | 使用分液漏斗和容量瓶时,先要检查是否漏液 |
1.下列关于化学用语的表述正确的是( )
| A. | 质量数为14的碳原子的表达式:${\;}_{8}^{14}$C | |
| B. | 乙醇的结构简式:C2H5OH | |
| C. | 乙烯的结构简式为CH2CH2 | |
| D. | 甲烷分子的球棍模型: |
18.将KCl和KBr的混合物13.4g溶于水配成500mL溶液,通入过量的Cl2,反应后将溶液蒸干,得到固体11.175g,则原来所配溶液中K+、Cl-、Br-的物质的量浓度之比为( )
| A. | 1:2:3 | B. | 1:3:2 | C. | 2:3:1 | D. | 3:2:1 |
15.设NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 0.1 L 3mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3NA | |
| B. | 1mol金刚石中含有的共价键数目为4NA | |
| C. | 1molNa2O2与足量的水反应,转移的电子数为2NA | |
| D. | 分子数为NA的CO、N2的混合气体在标准状况时体积约为22.4L,质量为28g |
9.在0.1mol•L-1 Na2CO3溶液中,欲使CO32-的浓度尽量接近0.1mol•L-1,则应向溶液中加( )
| A. | HCl | B. | Na2CO3 | C. | NaCl | D. | KOH |