题目内容
20.如表为元素周期表前四周期的一部分,下列有关A、B、C、D、E、F六种元素的叙述正确的是( )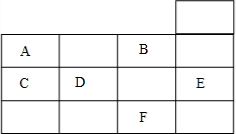
| A. | 常压下六种元素的单质中,F单质的沸点最高 | |
| B. | 晶体E中不存在化学键 | |
| C. | D元素的非金属性比B元素的非金属性强 | |
| D. | 单质A、C均没有同素异形体 |
分析 由元素在周期表中位置,可知A为N、B为F、C为P、D为S、E为Ar、F为Br.
A.根据单质的状态进行判断;
B.稀有气体为单原子分子;
C.同周期自左而右非金属性增强、同主族自上而下非金属性减弱;
D.磷的单质有红磷、白磷.
解答 解:由元素在周期表中位置,可知A为N、B为F、C为P、D为S、E为Ar、F为Br.
A.常温下氮气、氩为气体,磷、硫为固体,而Br2在常温下为液态,沸点不可能最高,故A错误;
B.氩为单原子分子,其晶体内无化学键,故B正确;
C.同周期自左而右非金属性增强、同主族自上而下非金属性减弱,故非金属性:F>S,故C错误;
D.磷的单质有红磷、白磷,存在同素异形体,故D错误,
故选:B.
点评 本题考查元素周期表与元素周期律,侧重对基础知识的巩固,注意对基础知识的积累着.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.关于苯乙烯(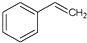 )的下列叙述,正确的是( )
)的下列叙述,正确的是( )
 )的下列叙述,正确的是( )
)的下列叙述,正确的是( )| A. | 苯乙烯不可能发生加成反应 | |
| B. | 苯乙烯不可能使酸性高锰酸钾溶液褪色 | |
| C. | 苯乙烯不可能使溴的四氯化碳溶液褪色 | |
| D. | 苯乙烯可通过加聚反应生成高分子化合物 |
8.下列说法不正确的是( )
| A. | 进行分液操作时,应先打开上口活塞或使塞上的凹槽对准漏斗口的小孔,然后打开旋塞,下层液体从下口放出,上层液体从漏斗上口倒出 | |
| B. | 纸层析法是以滤纸为惰性支持物,水为固定相,有机溶剂作流动相.用该方法可分离Fe3+和Cu2+,层析后氨熏显色,滤纸上方出现红棕色斑点 | |
| C. | 酸式滴定管、碱式滴定管、容量瓶、移液管都是准确量取一定体积液体的容器,它们在使用时都要进行检查是否漏水、水洗、润洗、注液、调整液面等几个过程 | |
| D. | 在制备硝酸钾晶体的实验中,趁热过滤时,承接滤液的小烧杯中预先加2mL蒸馏水.以防过滤时氯化钠晶体析出 |
15.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 42g乙烯和丙烯的混合气体中碳原子数目一定为3NA. | |
| B. | 用惰性电极电解CuSO4溶液后,如果加入0.1molCu(OH)2能使溶液复原,则电解时产生标准状况下1.12L的气体 | |
| C. | 配制一定物质的量浓度的NaOH溶液,把NaOH固体于烧杯中充分溶解,并迅速转移到容量瓶中定容 | |
| D. | 30g的NO与O2充分反应后,生成的气体分子数为1NA. |
5.下列不属于有机物的是( )
| A. | 氯化钠 | B. | 醋酸 | C. | 乙炔 | D. | 尿素 |
12.实验室制备少量硫酸亚铁晶体的实验步骤如下:①趁热过滤 ②洗涤、滤纸吸干 ③静置、冷却④水浴加热⑤抽滤 ⑥过量铁屑,加入20%-30%的稀硫酸溶液.则实验步骤正确的顺序为( )
| A. | ⑥⑤④①③② | B. | ⑥④⑤②①③ | C. | ⑥④①③⑤② | D. | ②⑥④①③⑤ |
9.下说法正确的是( )
| A. | 从海水中提取溴,富集溴可以用亚硫酸钠溶液或二氧化硫水溶液作为吸收液 | |
| B. | 从海水中提取碘常用过氧化氢做还原剂 | |
| C. | 可以用铝热反应制得单质镁 | |
| D. | 铝热剂就是指铝和氧化铁混合物 |



