题目内容
10.根据周期表对角线规则,回答下列问题:(1)写出Be(OH)2与盐酸和氢氧化钠溶液分别反应的离子方程式:Be(OH)2+2H+=Be2++2H2O,Be(OH)2+2OH-=BeO22-+2H2O.
(2)BeCl2溶液和MgCl2溶液可用试剂NaOH溶液加以鉴别,依据的实验现象是加入氢氧化钠生成沉淀,沉淀不溶解的为氯化镁,先生成沉淀后沉淀溶解的为氯化铍.
分析 (1)元素周期表中,处于对角线位置的元素具有相似的性质,则Be(OH)2与Al(OH)3的性质相似,与氢氧化钠反应生成Na2BeO2与水;
(2)氢氧化铍能和氢氧化钠反应,而Mg(OH)2和氢氧化钠不反应.
解答 解:(1)Be(OH)2与盐酸反应生成氯化铍和水,离子方程式为:Be(OH)2+2H+=Be2++2H2O,Be(OH)2与Al(OH)3的性质相似,与氢氧化钠反应生成Na2BeO2与水,反应离子方程式为:Be(OH)2+2OH-=BeO22-+2H2O,
故答案为:Be(OH)2+2H+=Be2++2H2O;Be(OH)2+2OH-=BeO22-+2H2O;
(2)氢氧化铍与氢氧化铝性质相似,能和氢氧化钠反应,而Mg(OH)2和氢氧化钠不反应,则选NaOH溶液鉴别,
故答案为:NaOH溶液;加入氢氧化钠生成沉淀,沉淀不溶解的为氯化镁,先生成沉淀后沉淀溶解的为氯化铍.
点评 本题考查元素周期表及应用,侧重学生分析能力及知识迁移应用能力的考查,利用已知物质的性质进行类比解答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.如表为元素周期表前四周期的一部分,下列有关A、B、C、D、E、F六种元素的叙述正确的是( )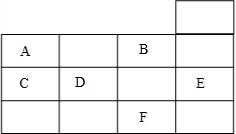

| A. | 常压下六种元素的单质中,F单质的沸点最高 | |
| B. | 晶体E中不存在化学键 | |
| C. | D元素的非金属性比B元素的非金属性强 | |
| D. | 单质A、C均没有同素异形体 |
1.某草药中有一种色素,它的结构简式为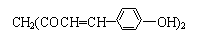 ,用它制成的试剂可以检验物质的酸碱性.能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是( )
,用它制成的试剂可以检验物质的酸碱性.能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是( )
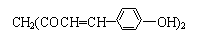 ,用它制成的试剂可以检验物质的酸碱性.能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是( )
,用它制成的试剂可以检验物质的酸碱性.能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是( )| A. | 3 mol、5 mol | B. | 6 mol、8 mol | C. | 10 mol、8 mol | D. | 6 mol、10 mol |
9.对于原子半径的理解,不正确的是( )
| A. | 同周期元素(除了稀有气体元素外),从左到右,原子半径依次减小 | |
| B. | 对于第三周期元素,从钠到氯,原子半径依次减小 | |
| C. | 各元素的原子半径总比其离子半径大 | |
| D. | 阴离子的半径大于其原子半径,阳离子的半径小于其原子半径 |
6.含有非极性共价键的物质是( )
| A. | H2 | B. | N2 | C. | SO2 | D. | NH3 |
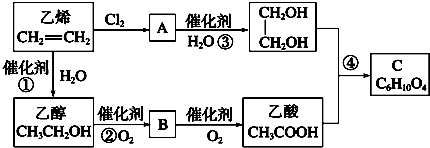
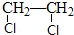 .
.