题目内容
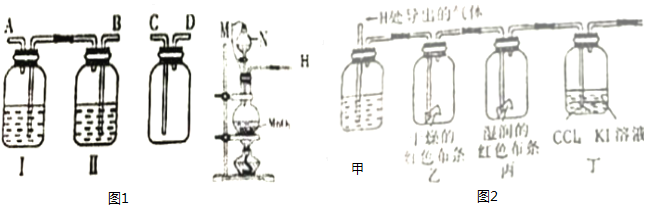
1.为了验证碳和浓硫酸反应的产物,某同学设计了如图所示实验装置:
(1)实验前要进行的操作是检查装置气密性.
(2)A中反应化学方程式是C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
(3)B中现象为无水硫酸铜变蓝,C装置的作用为检验是否生成SO2,E装置的作用为检验SO2是否被吸收完全.
分析 碳和浓硫酸反应生成二氧化碳、二氧化硫和水,无水硫酸铜检验水的存在,而品红溶液检验二氧化硫气,高锰酸钾除去二氧化硫气体,再通入品红溶液是验证二氧化硫是否除尽,最后通入澄清石灰水,验证二氧化碳气体的存在.
(1)气体发生和性质验证装置需要不漏气,开始前需要检验装置气密性;
(2)木炭和浓硫酸加热反应生成二氧化硫、二氧化碳和水;
(3)验证碳和浓硫酸反应的产物需要先验证生成的水,依据无水硫酸铜变蓝色说明生成水,再验证二氧化硫,能使品红试液褪色,除去二氧化硫后用澄清石灰验证二氧化碳.
解答 解:碳和浓硫酸反应生成二氧化碳、二氧化硫和水,无水硫酸铜检验水的存在,而品红溶液检验二氧化硫气,高锰酸钾除去二氧化硫气体,再通入品红溶液是验证二氧化硫是否除尽,最后通入澄清石灰水,验证二氧化碳气体的存在;
(1)气体发生和性质验证装置需要不漏气,开始前需要检验装置气密性,仪器按上图组装好后,首先应该进行的操作是检验装置气密性;
故答案为:检查装置气密性;
(2)木炭和浓硫酸加热反应生成二氧化硫、二氧化碳和水,反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;(1)检验装置气密性 (2)C+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O
(3)验证碳和浓硫酸反应的产物需要先验证生成的水,依据无水硫酸铜变蓝色说明生成水,再验证二氧化硫,能使品红试液褪色,除去二氧化硫后用澄清石灰验证二氧化碳;所以A中加入的试剂是无水硫酸铜,与水变化为蓝色,证明生成水;气体通入品红试液溶液褪色证明含有二氧化硫;再通入品红验证SO2是否被吸收完全,
故答案为:无水硫酸铜变蓝;检验是否生成SO2; 检验SO2是否被吸收完全.
点评 本题考查了浓硫酸性质的应用,产物验证方法和现象判断,注意二氧化碳、二氧化硫都可以使澄清石灰水变浑浊,题目难度中等.

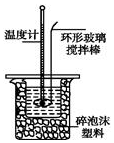 某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.Ⅰ.配制0.50mol•L-1NaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体5.0g.
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):abe.
| 名称 | 托盘天平 (带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是Cu传热快,热量损失大.
(2)在操作正确的前提下,提高中和热测定准确性的关键是减少实验过程中的热量损失.大烧杯如不盖硬纸板,求得的中和热数值将偏小(填“偏大”、“偏小”或“无影响”).结合日常生活实际该实验在保温杯中(家用产品)效果更好.
(3)写出该反应中和热的热化学方程式:(中和热为57.3kJ•mol-1)$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol;.
(4)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
| 试验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.6 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容c=4.18J•(g•℃)-1.则中和热△H=-53.5kJ/mol(取小数点后一位).
③上述实验数值结果与57.3kJ•mol-1有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
④实验中改用60mL0.5mol/L盐酸跟50mL0.55mol•L-1氢氧化钠进行反应,与上述实验相比,所放出的热量不相等(填相等或不相等,下同),所求的中和热相等简述理由中和热是指酸跟碱发生中和反应生成1mol水所放出的热量为标准的,而与酸、碱的用量无关..
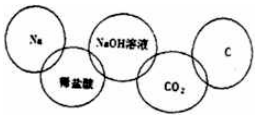 某同学在奥运五连环中填入5种物质 (如图所示),相连环的物质间发生的反应中,没有涉及的基本反应类型是( )
某同学在奥运五连环中填入5种物质 (如图所示),相连环的物质间发生的反应中,没有涉及的基本反应类型是( )| A. | 分解反应 | B. | 复分解反应 | C. | 化合反应 | D. | 置换反应 |
| A. | 硅在自然界中既有游离态又有化合态 | |
| B. | 高温下SiO2能与Na2CO3固体反应生成Na2SiO3和CO2,说明硅酸酸性强于碳酸 | |
| C. | 因为玻璃中含有SiO2,所以不能用磨口玻璃塞的试剂瓶盛装碱性溶液 | |
| D. | SiO2能与氢氧化钠溶液和氢氟酸反应,所以SiO2是两性氧化物 |
| A. | 电解质:胆矾、一水合氨、硫酸钡、CaO | |
| B. | 酸性氧化物:CO2、SO2、NO2、SiO2 | |
| C. | 混合物:铝热剂、干冰、水玻璃、盐酸 | |
| D. | 弱酸:氢碘酸、醋酸、碳酸、次氯酸 |
| A. | 葡萄酒中添加SO2,可起到抗氧化和抗菌的作用 | |
| B. | PM2.5颗粒分散到空气中可产生丁达尔效应 | |
| C. | 苯、四氯化碳、乙醇都可作萃取剂,也都能燃烧 | |
| D. | 淀粉、油脂、纤维素和蛋白质都是高分子化合物 |