题目内容
完成下列各题.
(1)镁是一种重要的金属,镁合金要用于制造火箭、导弹和飞机的部件等.工业上用电解熔融MgCl2可以得到金属镁,写出该反应的化学方程式
(2)在放电的条件下,空气中的N2和O2反应生成NO,写出该反应的化学方程式 .
(1)镁是一种重要的金属,镁合金要用于制造火箭、导弹和飞机的部件等.工业上用电解熔融MgCl2可以得到金属镁,写出该反应的化学方程式
(2)在放电的条件下,空气中的N2和O2反应生成NO,写出该反应的化学方程式
考点:镁的化学性质,氮的氧化物的性质及其对环境的影响
专题:元素及其化合物
分析:(1)用惰性电极电解熔融MgCl2时,阳极上氯离子放电、阴极上镁离子放电;
(2)在放电条件下,空气中的N2和O2反应生成NO,根据反应物、生成物及反应条件书写反应方程式.
(2)在放电条件下,空气中的N2和O2反应生成NO,根据反应物、生成物及反应条件书写反应方程式.
解答:
解:(1)用惰性电极电解熔融MgCl2时,阳极上氯离子放电、阴极上镁离子放电,反应方程式为MgCl2
Mg+Cl2↑,故答案为:MgCl2
Mg+Cl2↑;
(2)在放电条件下,空气中的N2和O2反应生成NO,根据反应物、生成物及反应条件知,该反应方程式为N2+O2
2NO,故答案为:N2+O2
2NO.
| ||
| ||
(2)在放电条件下,空气中的N2和O2反应生成NO,根据反应物、生成物及反应条件知,该反应方程式为N2+O2
| ||
| ||
点评:本题考查了反应方程式的书写,明确反应物、生成物及反应条件即可书写,注意(1)中电解氯化镁溶液和熔融氯化镁的区别,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某温度(t℃)时,水的离子积Kw=1×10-13,该温度下,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则混合之前,a与b之间应满足的关系是( )
| A、a+b=10 |
| B、a+b=12 |
| C、a+b=15 |
| D、a+b=16 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,5.6L氧气含有n个O2,则NA为4n |
| B、常温常压下,1mol氦气含有的原子数为2NA |
| C、常温下,1mol氧气和足量氢气反应,转移的电子数为2NA |
| D、18克水中所含的电子数为8NA |
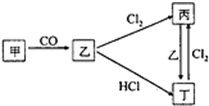 (已知甲、乙、丙、丁4种物质均含有常见金属元素A,其中甲为红棕色粉末.它们之间有如图所示的转化关系(转化过程申部分产物未标出).
(已知甲、乙、丙、丁4种物质均含有常见金属元素A,其中甲为红棕色粉末.它们之间有如图所示的转化关系(转化过程申部分产物未标出).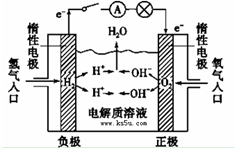 已知拆开1molH2需要消耗436kJ能量,拆开1molO2需要消耗496kJ能量,形成水分子中的1molH-O能够释放463kJ能量.根据以上所给的数据计算反应:
已知拆开1molH2需要消耗436kJ能量,拆开1molO2需要消耗496kJ能量,形成水分子中的1molH-O能够释放463kJ能量.根据以上所给的数据计算反应: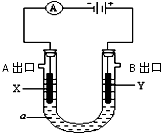 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板(X、Y都是惰性电极),A、B 是出口,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板(X、Y都是惰性电极),A、B 是出口,通过导线与直流电源相连.请回答以下问题: 某研究性学习小组欲探究原电池的形成条件,按下图所示装置进行实验
某研究性学习小组欲探究原电池的形成条件,按下图所示装置进行实验