题目内容
6.下列实验装置能达到实验目的是( )| A. |  进行喷泉实验 | B. |  加热熔融NaOH固体 | ||
| C. |  验证镁片与稀盐酸反应放热 | D. |  测定过氧化氢的纯度 |
分析 A.氯气在饱和食盐水中的溶解度比较小;
B.氢氧化钠能与二氧化硅反应;
C.升温氢氧化钙的溶解度变小;
D.排水法收集气体应短进长出.
解答 解:A.氯气在饱和食盐水中的溶解度比较小,不能形成气压差,故A错误;
B.氢氧化钠能与二氧化硅反应,应用铁坩埚,故B错误;
C.升温氢氧化钙的溶解度变小,析出沉淀,可验证,故C正确;
D.排水法收集气体应短进长出,无法将水排出,故D错误.
故选C.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.

练习册系列答案
相关题目
16.下列说法正确的是( )
| A. | 质子数为6,中子数为7的原子的元素符号可表示为${\;}_{6}^{13}$C | |
| B. | H2、SO2、CO三种气体都可用浓硫酸干燥 | |
| C. | 共价化合物溶于水,分子内共价键被破坏,单质溶于水,分子内共价键不被破坏 | |
| D. | 陶瓷、玻璃、水泥、大理石的主要成分都是硅酸盐 |
17.下列关于电解质溶液的叙述正确的是( )
| A. | pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | |
| B. | 在0.1mol•L-1 的NaHA溶液pH=4,则H2A为强酸 | |
| C. | 常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Clˉ)>c(NH4+)>c(H+)=c(OHˉ) | |
| D. | 向0.1mol•L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3•H2O)增大 |
14.金属Cu和一定浓度的HNO3反应:生成NO、NO2、N2O4,生成的气体恰好与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳在加热时反应,所产生的CO2的量( )
| A. | 小于0.5 mol | B. | 等于0.5 mol | C. | 大于0.5mol | D. | 无法确定 |
1.海水总量极大.金,铀等微量元素在海水中的总量自然也大,但从海水中获取这些微量元素的成本很高.其中成本最高的步骤在于( )
| A. | 从海水中富集含微量元素的化合物 | B. | 使含微量元素的离子沉淀 | ||
| C. | 对含微量元素的混合物进行提纯 | D. | 从化合物中冶炼这些单质 |
11.下列说法正确的是( )
| A. | 摩尔是物质质量的单位 | B. | 1 mol气体所占的体积一定是22.4L | ||
| C. | 1mol水质量为18g | D. | 氢气的摩尔质量是2g |
16.下列除去杂质的方法中正确的是( )
| A. | Cl2中混有少量HCl:通过盛有足量硝酸银溶液的洗气瓶洗气 | |
| B. | Cl2中混有少量水蒸气:先通过足量浓硫酸,再用向下排空气法收集氯气 | |
| C. | HCl中混有少量Cl2:通过盛有四氯化碳的洗气瓶洗气 | |
| D. | HCl中混有少量Cl2:通入足量氢气并光照 |
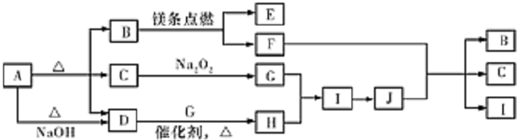
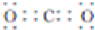 .
.